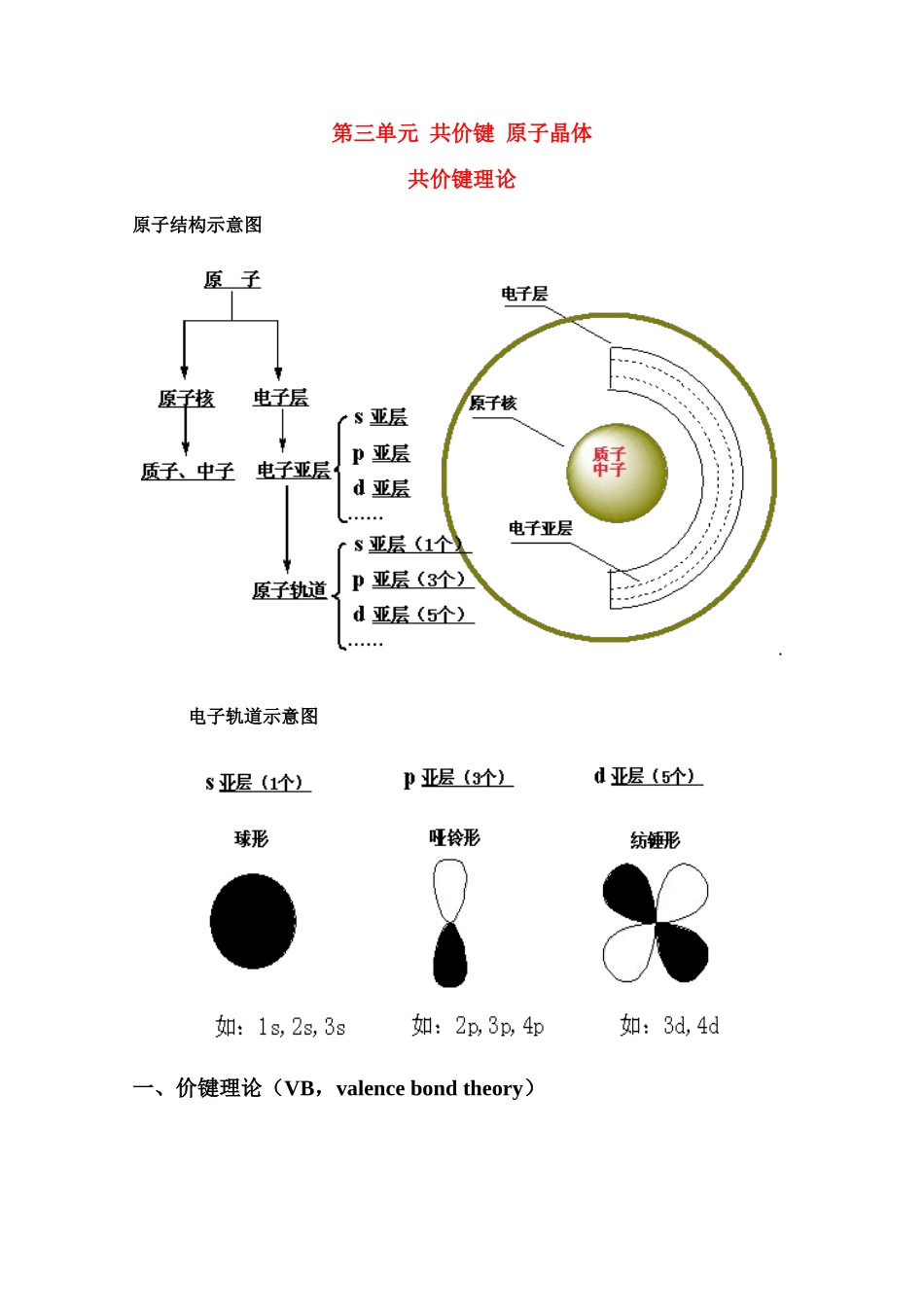
第三单元 共价键 原子晶体共价键理论原子结构示意图
电子轨道示意图 一、价键理论(VB,valence bond theory) 价键理论的三个要点:1
定域性:自旋反平行的两个电子绕核做高速运动,属于成键原子共同所有
电子对在两核之间出现的几率最大;2
饱和性:每个原子成键的总数或以单键连接的原子数目是一定的
原子中的成单电子数决定成键总数;3
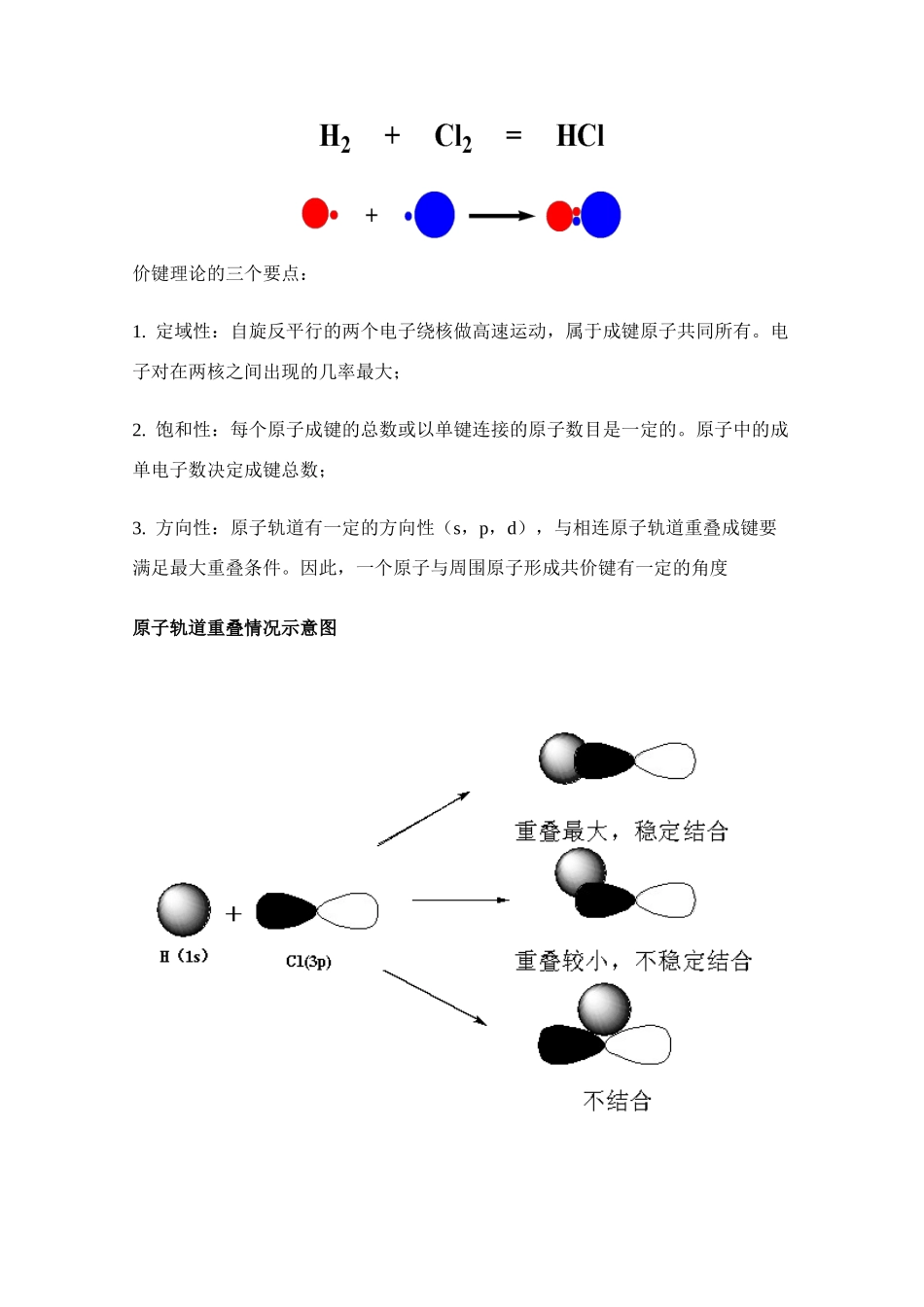
方向性:原子轨道有一定的方向性(s,p,d),与相连原子轨道重叠成键要满足最大重叠条件
因此,一个原子与周围原子形成共价键有一定的角度 原子轨道重叠情况示意图 成键方向对分子结构的影响 二、杂化轨道理论(hybrid orbital theory)1931 年,鲍林(Pauling L)提出原子轨道杂化理论
碳原子轨道的这种转化过程成为碳原子的杂化
杂化与杂化轨道:杂化是指在形成分子时,由于原子间的相互影响,若干不同类型而能量相近的原子轨道混合起来,重新组合成一组新轨道的过程
所形成的新轨道称为杂化轨道
孤立的原子不可能发生杂化,只有在形成分子的过程中才会发生
在杂化前后,原子轨道的数目保持不变
条件不同,杂化轨道类型可能不同
碳原子的杂化:(1)sp3 杂化:原子轨道在杂化过程中经过一个激发态 这是用一个 2s 轨道和三个 2p 轨道进行的杂化,故称为 sp3 杂化
与基态轨道相比,杂化轨道具有以下特点: a)
能量相等,成分相同(1/4s 轨道和 3/4p 轨道); b)
杂化轨道的电子云分布更集中,可使成键轨道间的重叠部分增大,成键能力增强; c)
sp3 杂化轨道在空间尽量伸展,呈最稳定正四面体型,轨道夹角 109°28′
sp3 杂化又称为正四面体杂化
(2)sp2 杂化:由 2s 轨道核两个 2p 轨道杂化,形成三个等同的 sp2 杂化轨道
另有一个 2p 轨道不参与杂化