影响化学反应速率的因素1.化学反应的本质是什么
该过程与能量有何关系
提示:化学反应的本质是旧键的断裂,新键的形成,断键吸收能量;成键释放能量
2.Mg、Al与同浓度盐酸反应,哪一个反应速率更快
提示:金属Mg与盐酸反应更快,因为Mg比Al的金属活动性更强,更容易与盐酸反应放出H2
3.通过《化学2》的学习,总结影响化学反应速率的外界因素有哪些
提示:影响化学反应速率的外界因素有浓度、温度、气体反应中压强、催化剂、反应物接触面积大小、固体反应物的颗粒大小等
[新知探究]探究1有效碰撞与化学反应的发生——反应物分子发生碰撞
——反应物分子之间发生有效碰撞
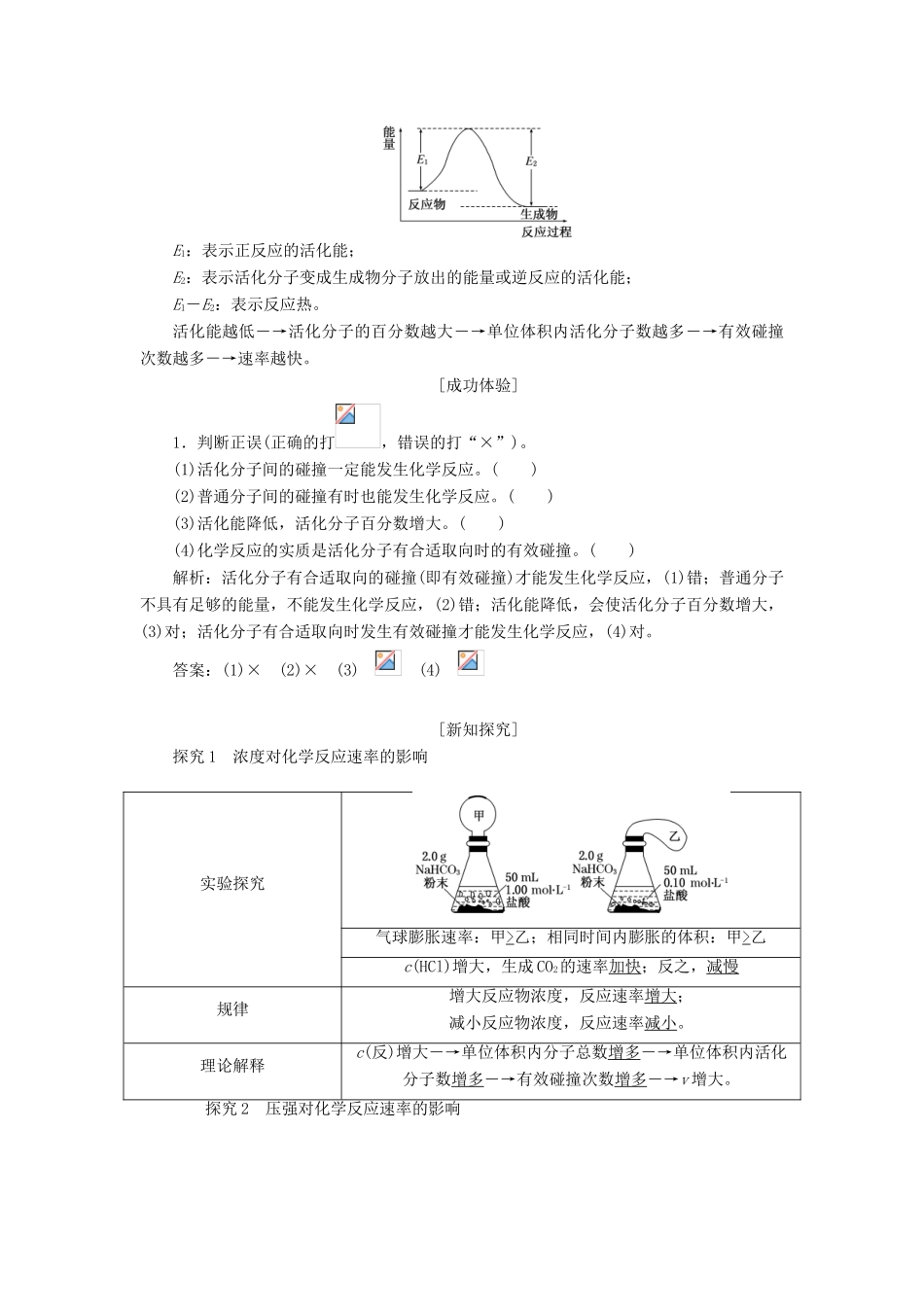
探究2有效碰撞理论[必记结论]1.分子的有效碰撞2.活化能与反应速率的关系E1:表示正反应的活化能;E2:表示活化分子变成生成物分子放出的能量或逆反应的活化能;E1-E2:表示反应热
活化能越低―→活化分子的百分数越大―→单位体积内活化分子数越多―→有效碰撞次数越多―→速率越快
[成功体验]1.判断正误(正确的打,错误的打“×”)
(1)活化分子间的碰撞一定能发生化学反应
()(2)普通分子间的碰撞有时也能发生化学反应
()(3)活化能降低,活化分子百分数增大
()(4)化学反应的实质是活化分子有合适取向时的有效碰撞
()解析:活化分子有合适取向的碰撞(即有效碰撞)才能发生化学反应,(1)错;普通分子不具有足够的能量,不能发生化学反应,(2)错;活化能降低,会使活化分子百分数增大,(3)对;活化分子有合适取向时发生有效碰撞才能发生化学反应,(4)对
答案:(1)×(2)×(3)(4)[新知探究]探究1浓度对化学反应速率的影响实验探究气球膨胀速率:甲>乙;相同时间内膨胀的体积:甲>乙c(HCl)增大,生成CO2的速率加快;反之,减慢规律增大反应物浓度,反应速率增大;减小反应物浓度,反应速率减小
理论解释c(反)增大