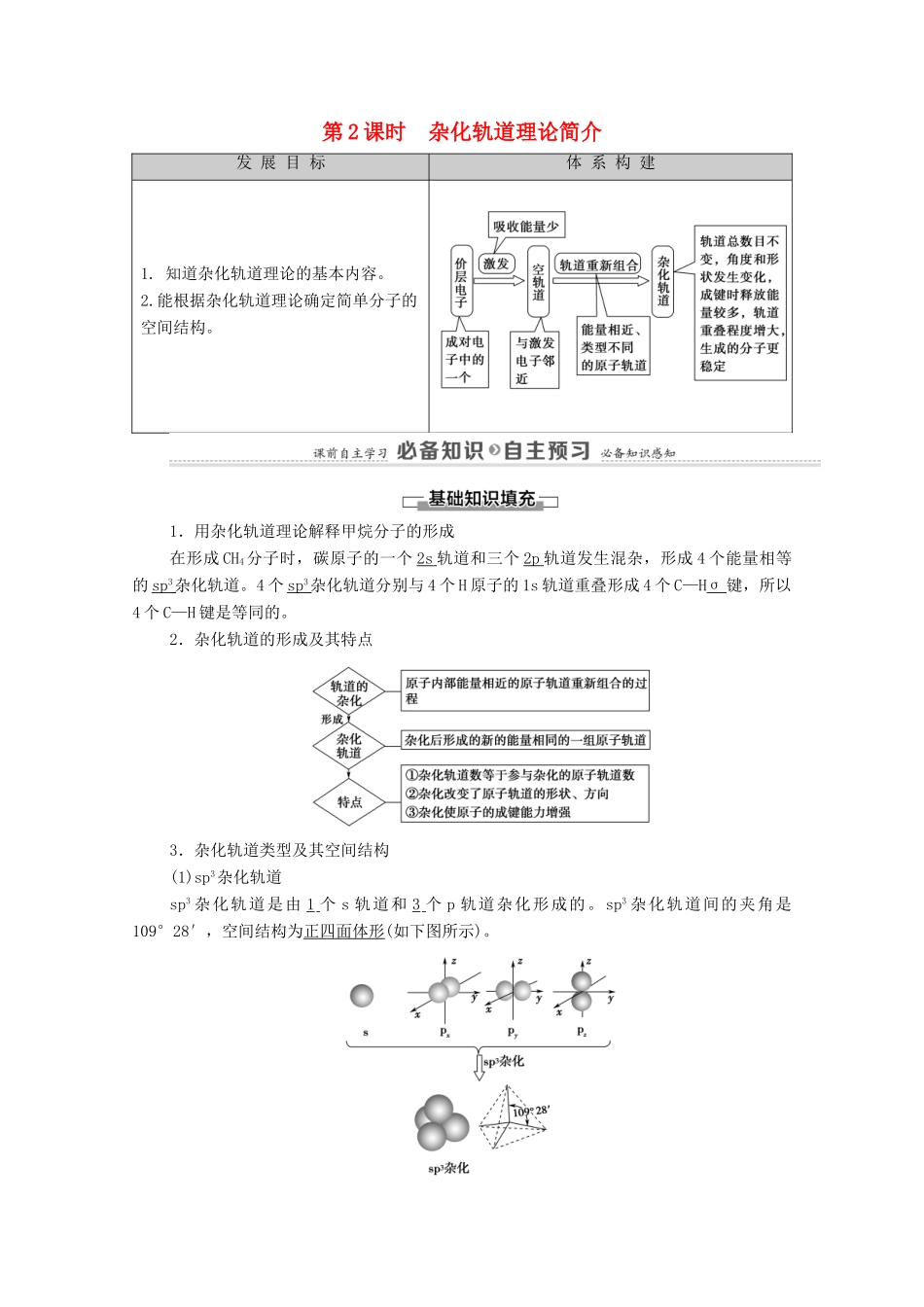
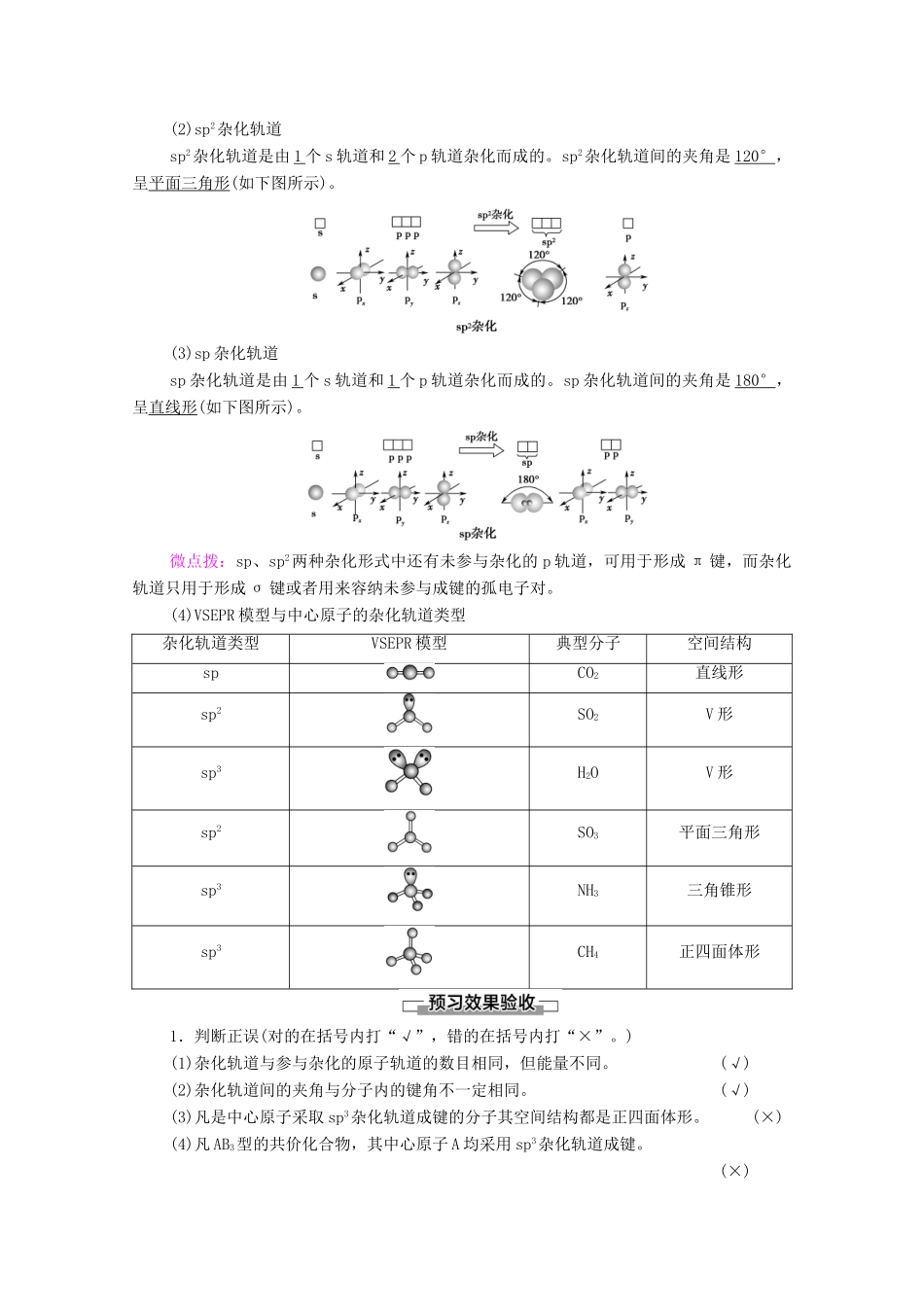
第2课时杂化轨道理论简介发展目标体系构建1.知道杂化轨道理论的基本内容。2.能根据杂化轨道理论确定简单分子的空间结构。1.用杂化轨道理论解释甲烷分子的形成在形成CH4分子时,碳原子的一个2s轨道和三个2p轨道发生混杂,形成4个能量相等的sp3杂化轨道。4个sp3杂化轨道分别与4个H原子的1s轨道重叠形成4个C—Hσ键,所以4个C—H键是等同的。2.杂化轨道的形成及其特点3.杂化轨道类型及其空间结构(1)sp3杂化轨道sp3杂化轨道是由1个s轨道和3个p轨道杂化形成的。sp3杂化轨道间的夹角是109°28′,空间结构为正四面体形(如下图所示)。(2)sp2杂化轨道sp2杂化轨道是由1个s轨道和2个p轨道杂化而成的。sp2杂化轨道间的夹角是120°,呈平面三角形(如下图所示)。(3)sp杂化轨道sp杂化轨道是由1个s轨道和1个p轨道杂化而成的。sp杂化轨道间的夹角是180°,呈直线形(如下图所示)。微点拨:sp、sp2两种杂化形式中还有未参与杂化的p轨道,可用于形成π键,而杂化轨道只用于形成σ键或者用来容纳未参与成键的孤电子对。(4)VSEPR模型与中心原子的杂化轨道类型杂化轨道类型VSEPR模型典型分子空间结构spCO2直线形sp2SO2V形sp3H2OV形sp2SO3平面三角形sp3NH3三角锥形sp3CH4正四面体形1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)(1)杂化轨道与参与杂化的原子轨道的数目相同,但能量不同。(√)(2)杂化轨道间的夹角与分子内的键角不一定相同。(√)(3)凡是中心原子采取sp3杂化轨道成键的分子其空间结构都是正四面体形。(×)(4)凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键。(×)2.能正确表示CH4中碳原子的成键方式的示意图为()D[碳原子的2s轨道与2p轨道形成4个等性的杂化轨道,因此碳原子4个价电子分占在4个sp3杂化轨道上,且自旋状态相同。]3.ClO-、ClO、ClO、ClO中,中心原子Cl都是以sp3杂化轨道方式与O原子成键,则ClO-的空间结构是________;ClO的空间结构是________;ClO的空间结构是________;ClO的空间结构是________。[解析]ClO-的组成决定其空间结构为直线形。其他3种离子的中心原子的杂化方式都为sp3杂化,从离子的组成上看其空间结构依次类似于H2O、NH3、CH4(或NH)。[答案]直线形V形三角锥形正四面体形杂化类型及分子空间结构的判断在形成多原子分子时,中心原子价电子层上的某些能量相近的原子轨道发生混杂,重新组合成一组新的轨道的过程,叫做轨道的杂化。双原子分子中,不存在杂化过程。例如sp杂化、sp2杂化的过程如下:(1)观察上述杂化过程,分析原子轨道杂化后,数量和能量有什么变化?提示:杂化轨道与参与杂化的原子轨道数目相同,但能量不同。s轨道与p轨道的能量不同,杂化后,形成的一组杂化轨道能量相同。(2)2s轨道与3p轨道能否形成sp2杂化轨道?提示:不能。只有能量相近的原子轨道才能形成杂化轨道。2s与3p不在同一能级,能量相差较大。(3)用杂化轨道理论解释NH3、H2O的空间结构?提示:NH3分子中N原子的价电子排布式为2s22p3。1个2s轨道和3个2p经杂化后形成4个sp3杂化轨道,其中3个杂化轨道中各有1个未成对电子,分别与H原子的1s轨道形成共价键,另1个杂化轨道中是成对电子,不与H原子形成共价键,sp3杂化轨道为正四面体形,但由于孤电子对的排斥作用,使3个N—H的键角变小,成为三角锥形的空间结构。H2O分子中O原子的价电子排布式为2s22p4。1个2s轨道和3个2p轨道经杂化后形成4个sp3杂化轨道,其中2个杂化轨道中各有1个未成对电子,分别与H原子的1s轨道形成共价键,另2个杂化轨道是成对电子,不与H原子形成共价键,sp3杂化轨道为正四面体形,但由于2对孤电子对的排斥作用,使2个O—H的键角变得更小,成为V形的空间结构。(4)CH4、NH3、H2O中心原子的杂化类型都为sp3,键角为什么依次减小?从杂化轨道理论的角度比较键角大小时有什么方法?提示:CH4、NH3、H2O中心原子都采取sp3杂化,中心原子的孤电子对数依次为0个、1个、2个。由于孤电子对对共用电子对的排斥作用使键角变小,孤电子对数越多排斥作用越大,键角越小。比较键角时,先看中心原子杂化类型,杂化类型不同时:一般键角按sp、sp2、sp3顺序依次减小;杂化类型相同时,中心原子孤电子对数越...