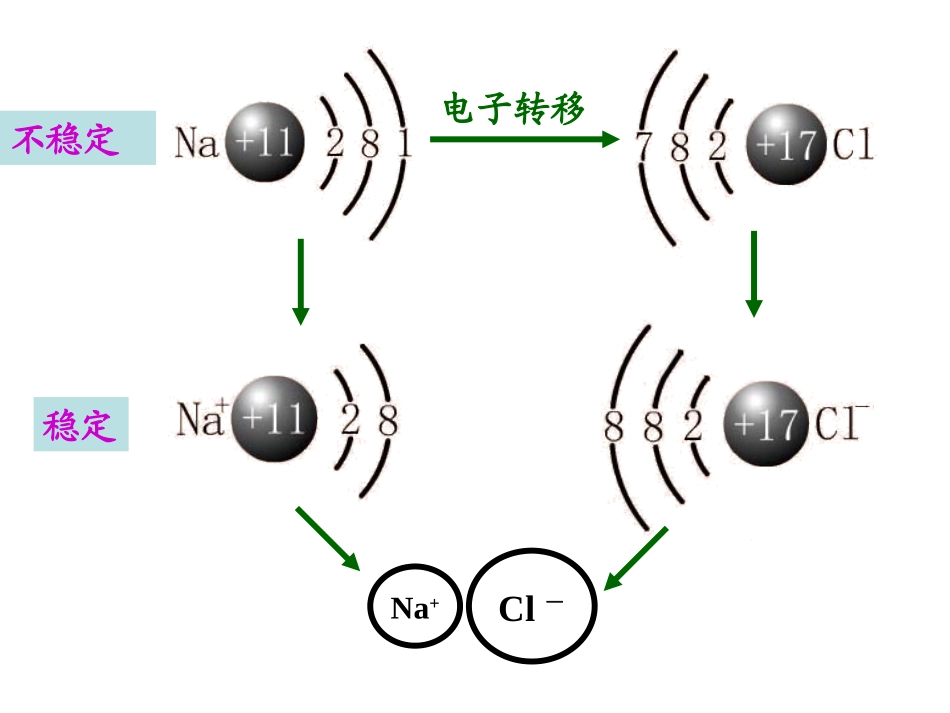
第三节化学键Na+Cl-电子转移不稳定稳定在氯化钠晶体中,Na+和Cl-间存在哪些力
1、Na+离子和Cl-离子间的静电吸引作用2、电子与电子、原子核与原子核间的静电斥力作用思考思考一
离子键阴阳离子接近到某一定距离时,吸引和排斥达到平衡,就形成了离子键
成键过程:1
定义:带相反电荷离子之间的相互作用称为离子键由离子键构成的化合物叫做离子化合物
成键原因:成键粒子:成键本质:成键元素:电子得失阴阳离子静电作用(静电吸引和静电排斥)活泼的金属元素(ⅠA,ⅡA)和活泼的非金属元素(ⅥA,ⅦA)思考思考哪些物质中存在离子键呢
2、活泼的金属元素和酸根离子形成的盐,即大部分盐
(如:NaNO3)3、铵根和酸根离子(或活泼非金属元素)形成的盐
(如:NH4Cl,(NH4)2SO4)1、活泼的金属元素和活泼的非金属元素之间的化合物
(如:Na2O.Na2O2)4、金属阳离子与OH-(如NaOH),即强碱
(IA、IIA)(VIA、VIIA)2
离子化合物:由离子键构成的化合物
二.电子式a
原子的电子式:在元素符号周围用小黑点·(或×)来表示原子的最外层电子
这种式子叫做电子式
H×Na××Mg×b
离子的电子式:[]×[]2-××—Na+Mg2+归纳:电子式是怎样写的
(1)原子的电子式:常把其最外层电子数用小黑点“
”或小叉“×”来表示
电子式H·(2)简单阳离子的电子式:就是其离子符号,不要求画出离子最外层电子数
Na+Mg2+(3)简单阴离子的电子式:不但要画出最外层电子数,而且还应用中括号“[]”括起来,并在右上角标出“n-”电荷字样
····[O]2-::[Cl]-····::书写要点AB型AB2型A2B型(4)离子化合物的电子式:由阴、阳离子的电子式组成,但对相同离子不能合并
NaClMgCl2Na2S注意:相同的离子不能写在一起,一般对称排列
[练习]写出下