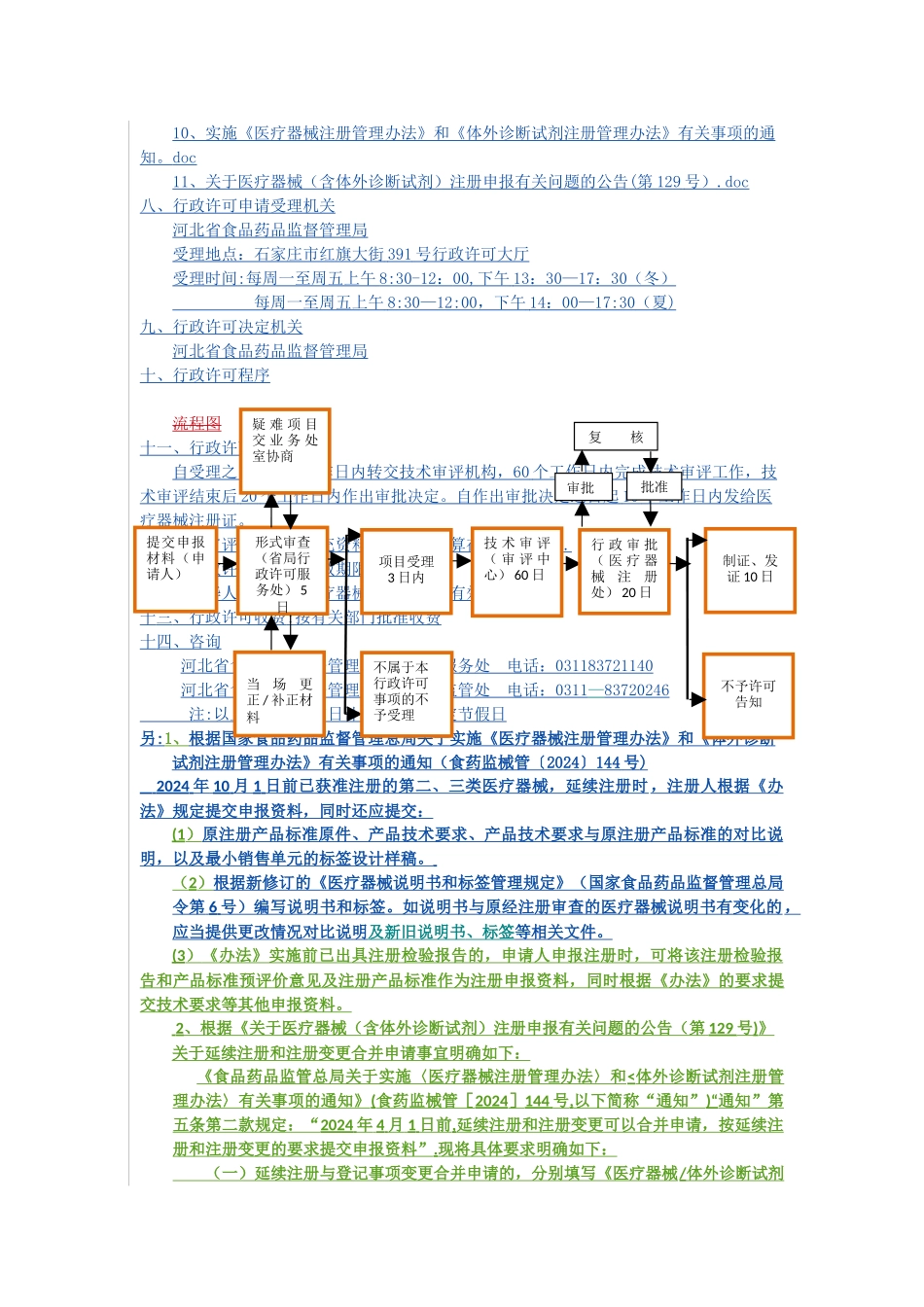
二类有源、无源类医疗器械延续注册办事指南一、许可事项名称:《医疗器械注册证》延续二、行政许可内容二类有源、无源类医疗器械延续注册受理及审批三、法定依据: 1、《行政许可法》2、《医疗器械监督管理条例》(国务院令第 650 号) 2、《医疗器械注册管理办法》(国家食品药品监督管理总局令第 4 号 ) 五、行政许可条件(一)原医疗器械注册证为广东河北省食品药品监督管理局核发且申请时根据第二类医疗器械管理的。(二)注册证有效期届满 6 个月前申请延续注册。(三)申请符合《医疗器械注册管理办法》规定。(四)有下列情形之一的,不予延续注册:1。注册人未在规定期限内提出延续注册申请的;2。医疗器械强制性标准已经修订,该医疗器械不能达到新要求的;3.对用于治疗罕见疾病以及应对突发公共卫生事件急需的医疗器械,批准注册部门在批准上市时提出要求,注册人未在规定期限内完成医疗器械注册证载明事项的。六、申请材料目录(一)申请表(二)证明性文件(三)关于产品没有变化的声明(四)原医疗器械注册证及附件复印件、相应的历次医疗器械注册变更文件复印件。(五)注册证有效期内产品质量分析报告(六)产品检验报告(七)符合性声明(八)行政许可申请书(九)其他七、申请材料要求(一)格式及其他要求(1)申请材料应清楚、干净,使用 A4 规格纸张打印;(2)每项文件第一页作标签,或用带标签的隔页纸分隔,并按申请材料一级目录标明项目编号;(3)每项文件均应加盖企业公章;(4)根据申请材料目录的顺序装订成册;(5)办理医疗器械注册申请事务的人员应当受申请人委托,应出示授权委托书及该办理人身份证明原件与复印件.(6)申报资料(含检验报告)中所有文件在原件提交并受理后,再次提交时,可提交复印件并标注原件出处.(7)延续注册时注册人无法提交原注册产品标准原件的,应提交原注册产品标准复印件、无法提交原件的原因说明及所提交复印件与原件一致的声明。(二)申请材料具体要求1。申请表2.证明性文件注册人提供企业营业执照的副本复印件和组织机构代码证复印件;3。关于产品没有变化的声明注册人提供产品没有变化的声明(注册证及其变更文件中载明的内容、产品所涉及的相关国家标准和行业标准没有修订或没有新的相关国家标准和行业标准发布、影响产品安全有效的设计、原材料、生产工艺、适用范围、使用方法等).4。原医疗器械注册证及附件复印件、相应的历次医疗器械注册变更文件复印件。5。注册证有效期内产品质量分...