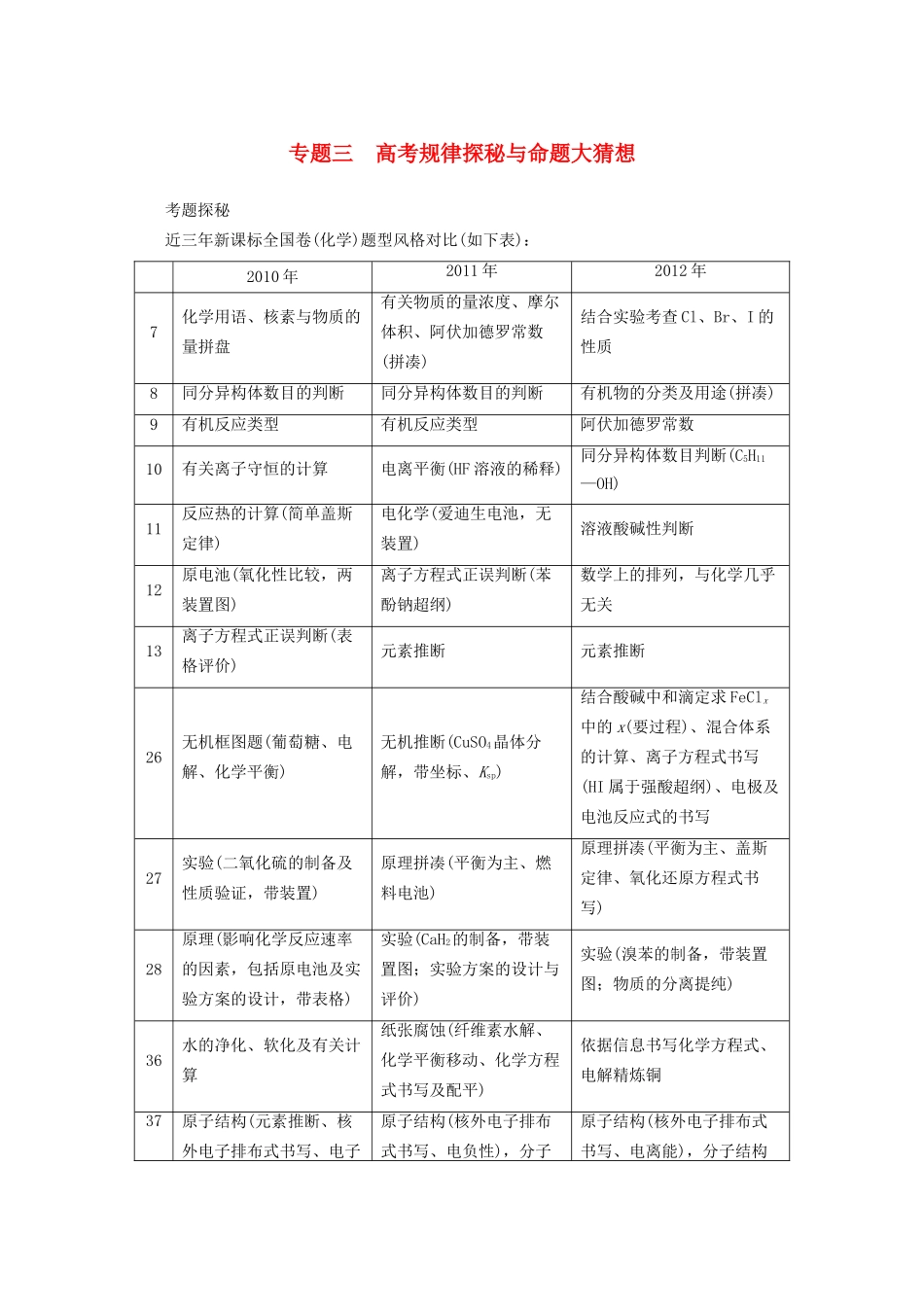
专题三高考规律探秘与命题大猜想考题探秘近三年新课标全国卷(化学)题型风格对比(如下表):2010年2011年2012年7化学用语、核素与物质的量拼盘有关物质的量浓度、摩尔体积、阿伏加德罗常数(拼凑)结合实验考查Cl、Br、I的性质8同分异构体数目的判断同分异构体数目的判断有机物的分类及用途(拼凑)9有机反应类型有机反应类型阿伏加德罗常数10有关离子守恒的计算电离平衡(HF溶液的稀释)同分异构体数目判断(C5H11—OH)11反应热的计算(简单盖斯定律)电化学(爱迪生电池,无装置)溶液酸碱性判断12原电池(氧化性比较,两装置图)离子方程式正误判断(苯酚钠超纲)数学上的排列,与化学几乎无关13离子方程式正误判断(表格评价)元素推断元素推断26无机框图题(葡萄糖、电解、化学平衡)无机推断(CuSO4晶体分解,带坐标、Ksp)结合酸碱中和滴定求FeClx中的x(要过程)、混合体系的计算、离子方程式书写(HI属于强酸超纲)、电极及电池反应式的书写27实验(二氧化硫的制备及性质验证,带装置)原理拼凑(平衡为主、燃料电池)原理拼凑(平衡为主、盖斯定律、氧化还原方程式书写)28原理(影响化学反应速率的因素,包括原电池及实验方案的设计,带表格)实验(CaH2的制备,带装置图;实验方案的设计与评价)实验(溴苯的制备,带装置图;物质的分离提纯)36水的净化、软化及有关计算纸张腐蚀(纤维素水解、化学平衡移动、化学方程式书写及配平)依据信息书写化学方程式、电解精炼铜37原子结构(元素推断、核外电子排布式书写、电子原子结构(核外电子排布式书写、电负性),分子原子结构(核外电子排布式书写、电离能),分子结构跃迁),分子结构(空间构型、杂化方式),晶体结构(熔沸点、晶胞的计算)结构(空间构型、杂化方式),晶胞的计算(无晶胞图)(空间构型、性质),晶胞的计算(带晶胞图、较难)38有机推断(名称、同分异构体数