第1课时金属晶体离子晶体发展目标体系构建1
能借助金属晶体结构模型认识金属晶体的结构特点
能利用形成晶体的作用力解释金属的性质
2.认识几种常见离子晶体的模型,并能解释离子晶体的性质
一、金属晶体1.金属晶体的概念点拨:金属晶体中因金属键的存在使得金属具有良好的延展性和可塑性
2.常见金属晶体的结构常见金属Ca、Cu、Au、Al、Pd、Pt、AgLi、Na、K、Ba、W、FeMg、Zn、Ti结构示意图(1)金属在发生变形延展时,金属键断裂吗
提示:不断裂
(2)金属在通常状况下都是晶体吗
金属晶体的性质与哪些因素有关
提示:不是,如汞;金属键和金属原子的堆积方式决定金属的性质
二、离子晶体1.概念阴、阳离子通过离子键结合,在空间呈现周期性重复排列所形成的晶体
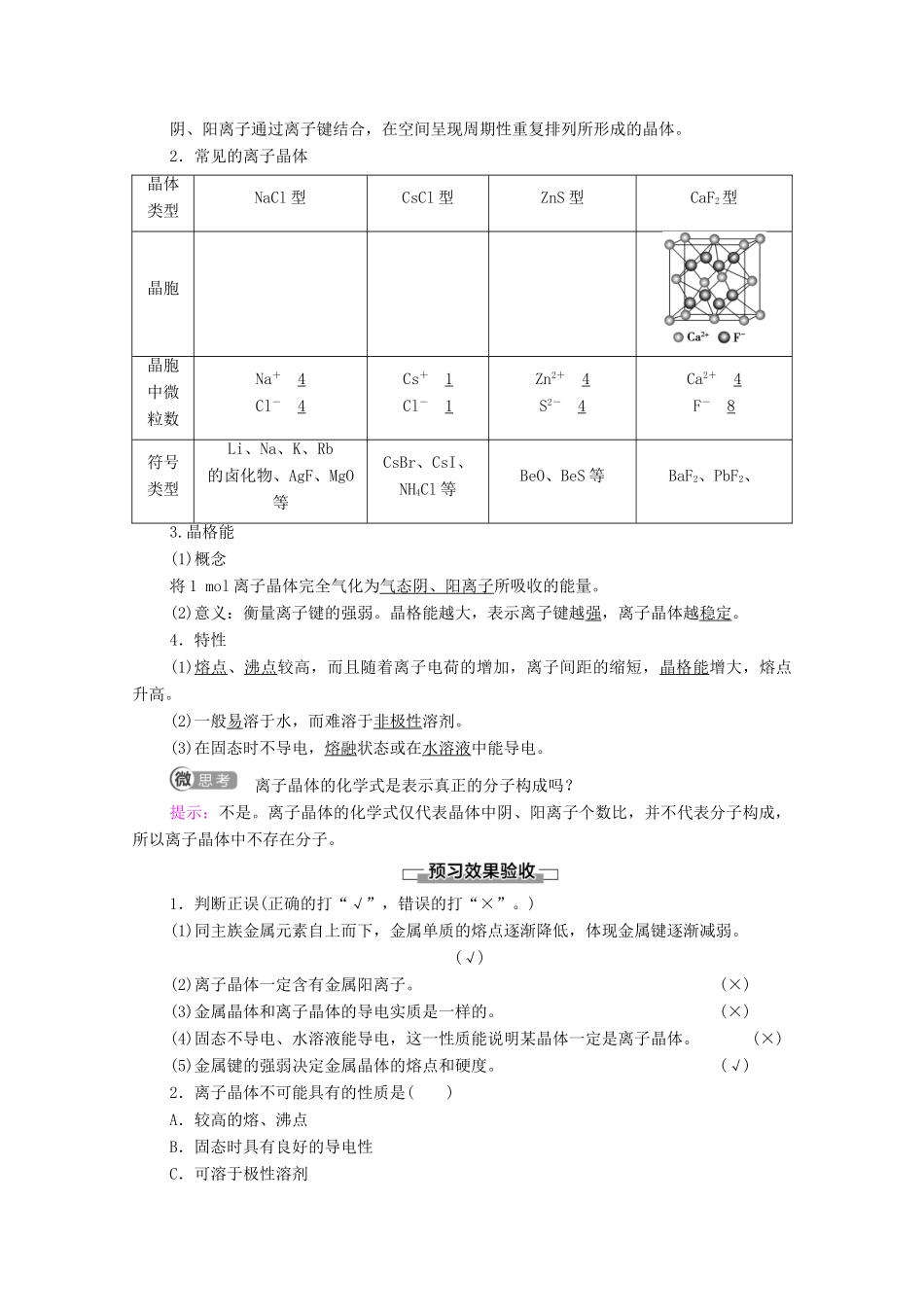
2.常见的离子晶体晶体类型NaCl型CsCl型ZnS型CaF2型晶胞晶胞中微粒数Na+4Cl-4Cs+1Cl-1Zn2+4S2-4Ca2+4F-8符号类型Li、Na、K、Rb的卤化物、AgF、MgO等CsBr、CsI、NH4Cl等BeO、BeS等BaF2、PbF2、3
晶格能(1)概念将1mol离子晶体完全气化为气态阴、阳离子所吸收的能量
(2)意义:衡量离子键的强弱
晶格能越大,表示离子键越强,离子晶体越稳定
4.特性(1)熔点、沸点较高,而且随着离子电荷的增加,离子间距的缩短,晶格能增大,熔点升高
(2)一般易溶于水,而难溶于非极性溶剂
(3)在固态时不导电,熔融状态或在水溶液中能导电
离子晶体的化学式是表示真正的分子构成吗
离子晶体的化学式仅代表晶体中阴、阳离子个数比,并不代表分子构成,所以离子晶体中不存在分子
1.判断正误(正确的打“√”,错误的打“×”
)(1)同主族金属元素自上而下,金属单质的熔点逐渐降低,体现金属键逐渐减弱
(√)(2)离子晶体一定含有金属阳离子
(×)(3)金属晶体和离子晶体