年级高三学科化学版本苏教版内容标题高三其次轮复习:分子结构与晶体结构【本讲教化信息】一
教学内容:分子结构与晶体结构二
教学目标了解化学键的含义,理解并驾驭共价键的主要类型及特点,共价键、离子键及金属键的主要区分及对物质性质的影响
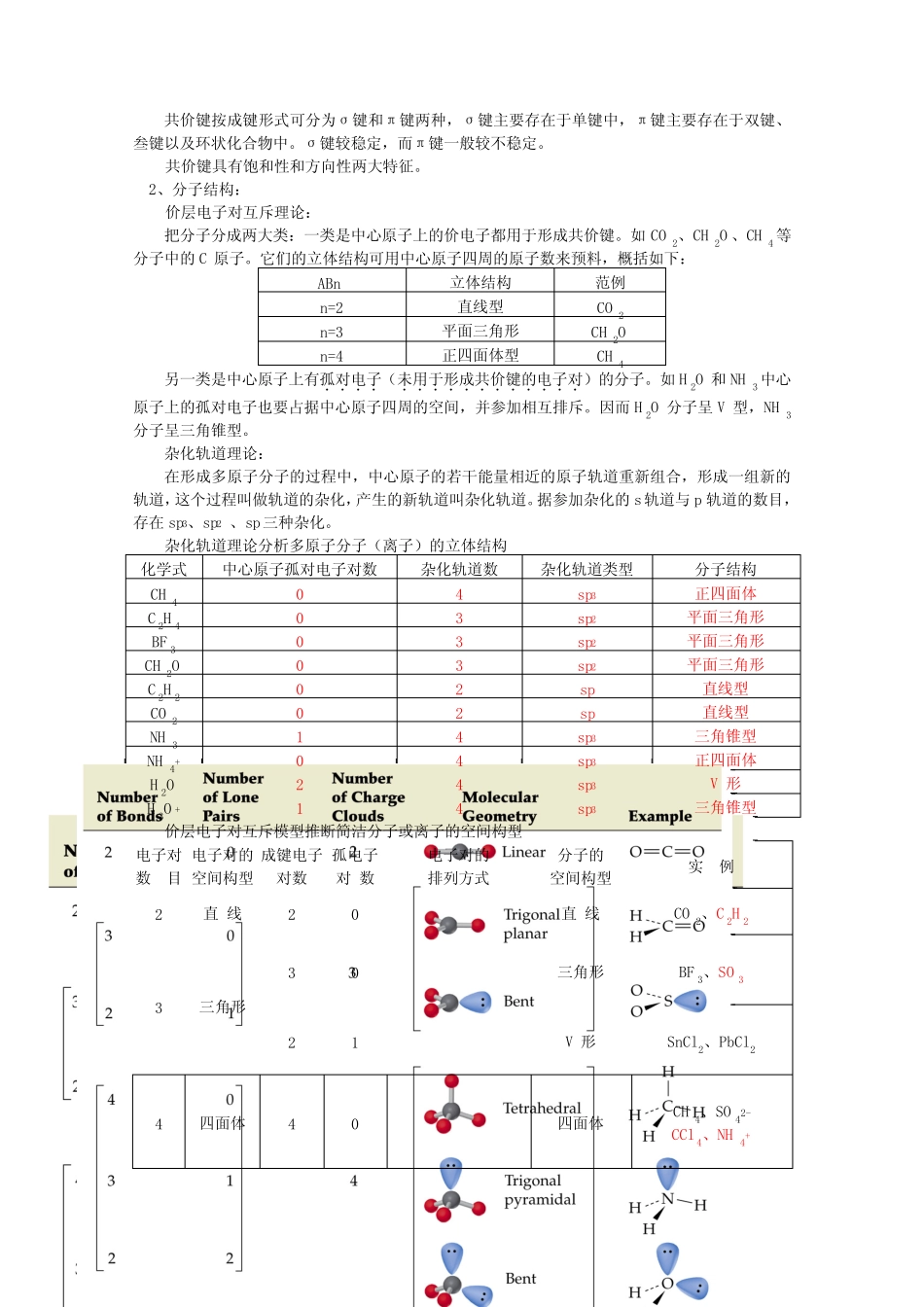
能依据杂化轨道理论和价层电子对互斥模型推断简洁分子或离子的空间构型,了解等电子体的含义
了解原子晶体、分子晶体和金属晶体的结构特征,驾驭不同晶体的构成微粒及微粒间的相互作用力,驾驭影响晶体熔沸点、溶解性的因素
教学重点、难点分子结构与晶体结构的特点,影响物质熔沸点和溶解性、酸性的因素四
教学过程(一)化学键与分子结构:1、化学键:相邻的两个或多个原子之间剧烈的相互作用,通常叫做化学键
三种化学键的比较:离子键共价键金属键形成过程阴阳离子间的静电作用原子间通过共用电子对所形成的相互作用金属阳离子与自由电子间的相互作用构成元素典型金属(含NH4+)和典型非金属、含氧酸根非金属金属实例离子化合物,如典型金属氧化物、强碱、大多数盐多原子非金属单质、气态氢化物、非金属氧化物、酸等金属配位键:配位键属于共价键,它是由一方供应孤对电子,另一方供应空轨道所形成的共价键,例如:NH4+的形成在NH4+中,虽然有一个N-H键形成过程与其它3个N-H键形成过程不同,但是一旦形成之后,4个共价键就完全相同
共价键的三个键参数概念意义键长分子中两个成键原子核间距离(米)键长越短,化学键越强,形成的分子越稳定键能对于气态双原子分子AB,拆开1molA-B键所需的能量键能越大,化学键越强,越坚固,形成的分子越稳定键角键与键之间的夹角键角确定分子空间构型键长、键能确定共价键的强弱和分子的稳定性:原子半径越小,键长越短,键能越大,分子越稳定
共价键的极性极性键非极性键共用电子对偏移程度偏移不偏移构成元素不同种非金属元素同种非金属元素实例HCl、H2O、CO2、H2SO4H2、