第一节原电池目标与素养:1
以铜锌原电池为例,了解原电池的工作原理
(宏观辨识与变化观念)2
会正确判断原电池的正极和负极,能正确书写电极反应式和电池反应方程式
(科学探究与模型认知)3
了解原电池原理的应用
(科学精神与社会责任)一、原电池工作原理1.概念:将化学能转化为电能的装置,称为原电池,其反应实质是自发的氧化还原反应
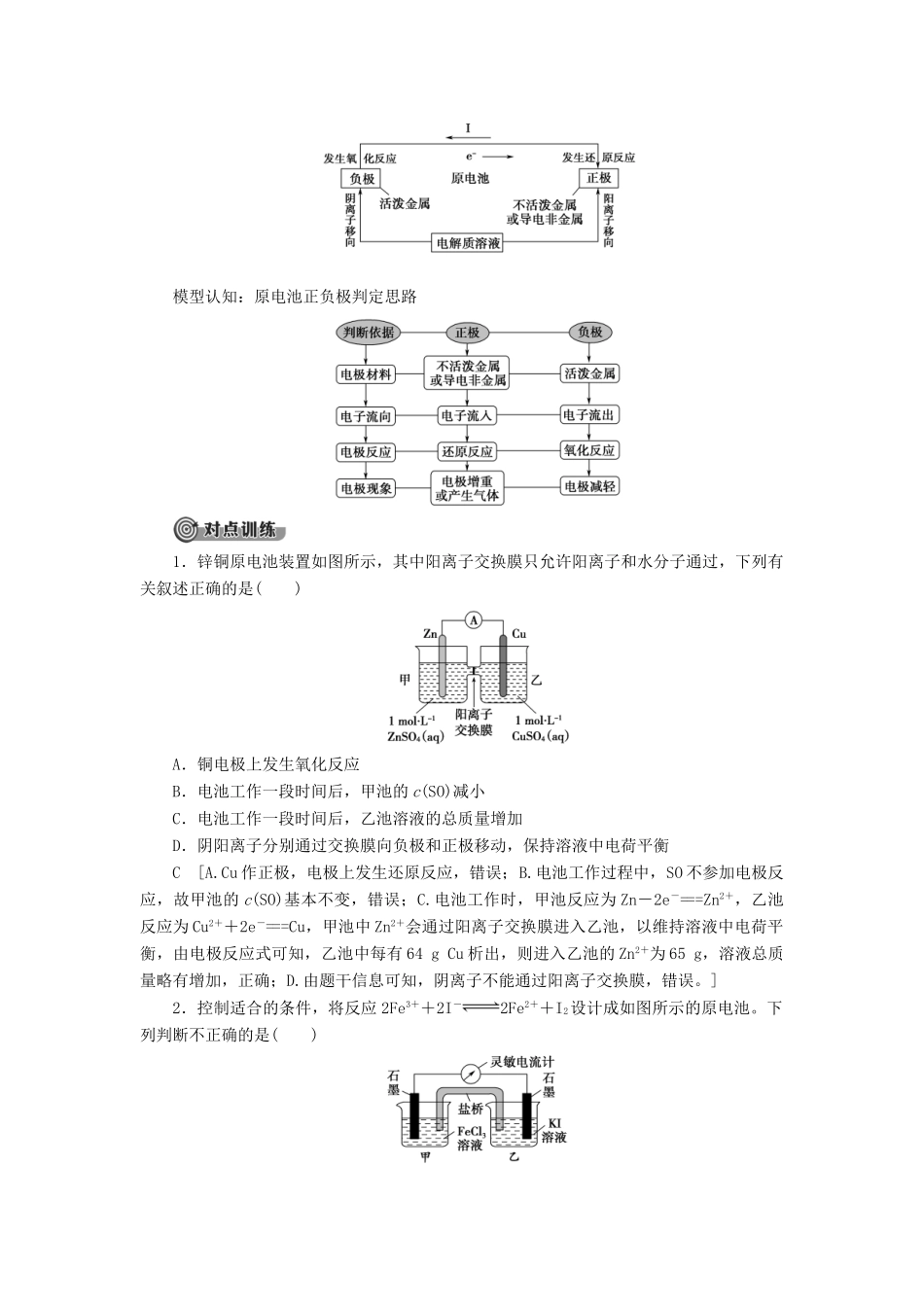
2.锌铜原电池工作原理装置与现象锌片逐渐溶解,铜片上有红色物质析出,电流表指针发生偏转电极名称Zn电极—负极Cu电极—正极得失电子失电子得电子电子流向流出流入反应类型氧化反应还原反应电极反应式Zn-2e-===Zn2+Cu2++2e-===Cu总反应式Zn+Cu2+===Zn2++Cu3.盐桥(1)成分:含有琼胶的KCl饱和溶液
(2)离子移动方向:Cl-移向负极区,K+移向正极区
微点拨:盐桥作用:①通过离子在盐桥中的定向移动,使两个隔离的电解质溶液连接起来,可使电流持续传导
②将两个半电池完全隔开,使副反应减至最低程度,可以获得单纯的电极反应,有利于最大程度地将化学能转化为电能
提高原电池效率
4.原电池的构成条件二、原电池的设计1.原电池的组成:原电池是由两个半电池组成,如锌铜原电池是锌半电池和铜半电池通过盐桥连接
2.原电池设计关键(1)外电路负极(还原性较强的物质)――→正极(较稳定的金属或能导电的非金属)
(2)内电路将两极浸入电解质溶液中,使阴、阳离子做定向移动
阴离子移向负极,阳离子移向正极
1.判断正误(正确的打“√”,错误的打“×”)(1)任何自发的放热反应均可设计原电池反应
()(2)原电池反应将氧化反应和还原反应分在不同区域同时进行
()(3)盐桥中的阴离子移向正极区域,使正极区溶液呈电中性
()(4)Fe—CuSO4(aq)—Cu形成的原电池的负极反应为Fe-3e-===Fe3+
()[答案](1)×(2)√(3)×(4)×