影响化学反应速率的因素[核心素养发展目标]1
宏观辨识与微观探析:通过实验,从宏观上认识外界因素影响化学反应速率的规律,并能从活化分子的有效碰撞等微观的角度进行分析解释
证据推理与模型认知:建立分析探究外界因素影响化学反应速率的思维模型,即“实验现象→影响规律→理论解释”,促进“证据推理”核心素养的发展
一、有效碰撞理论1.有效碰撞2.活化能和活化分子(1)活化分子:能够发生有效碰撞的分子
(2)活化能:活化分子所多出的那部分能量(或普通分子转化成活化分子所需要的能量)
3.反应物、生成物的能量与活化能的关系图反应的活化能越低,活化分子百分数越大,反应速率越快
例1下列说法正确的是()A.活化分子具有的能量是活化能B.活化分子的总数越多,反应速率越快C.某一反应的活化分子的百分数是个定值D.单位时间内有效碰撞次数越多,反应速率越快答案D解析活化分子具有的平均能量与普通分子具有的平均能量之差才叫活化能,A项错误;单位体积内活化分子总数越多,有效碰撞机会越多,反应速率才越快,B项错误;只有在一定条件下,活化分子在反应物中所占百分数才是定值,C项错误
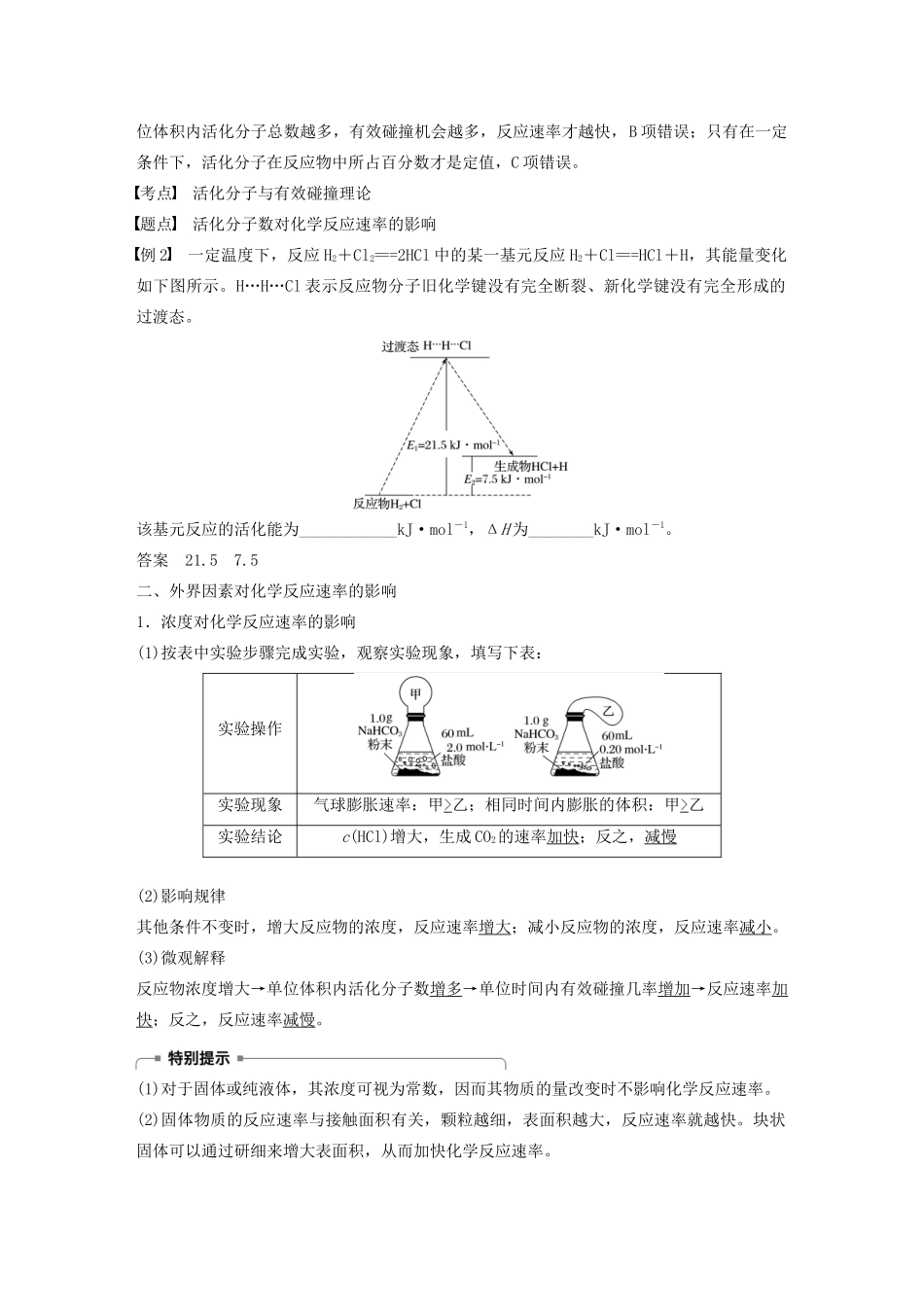
考点活化分子与有效碰撞理论题点活化分子数对化学反应速率的影响例2一定温度下,反应H2+Cl2===2HCl中的某一基元反应H2+Cl===HCl+H,其能量变化如下图所示
H…H…Cl表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态
该基元反应的活化能为____________kJ·mol-1,ΔH为________kJ·mol-1
5二、外界因素对化学反应速率的影响1.浓度对化学反应速率的影响(1)按表中实验步骤完成实验,观察实验现象,填写下表:实验操作实验现象气球膨胀速率:甲>乙;相同时间内膨胀的体积:甲>乙实验结论c(HCl)增大,生成CO2的速率加快;反之,减慢(2)影响规律其他条件不变时