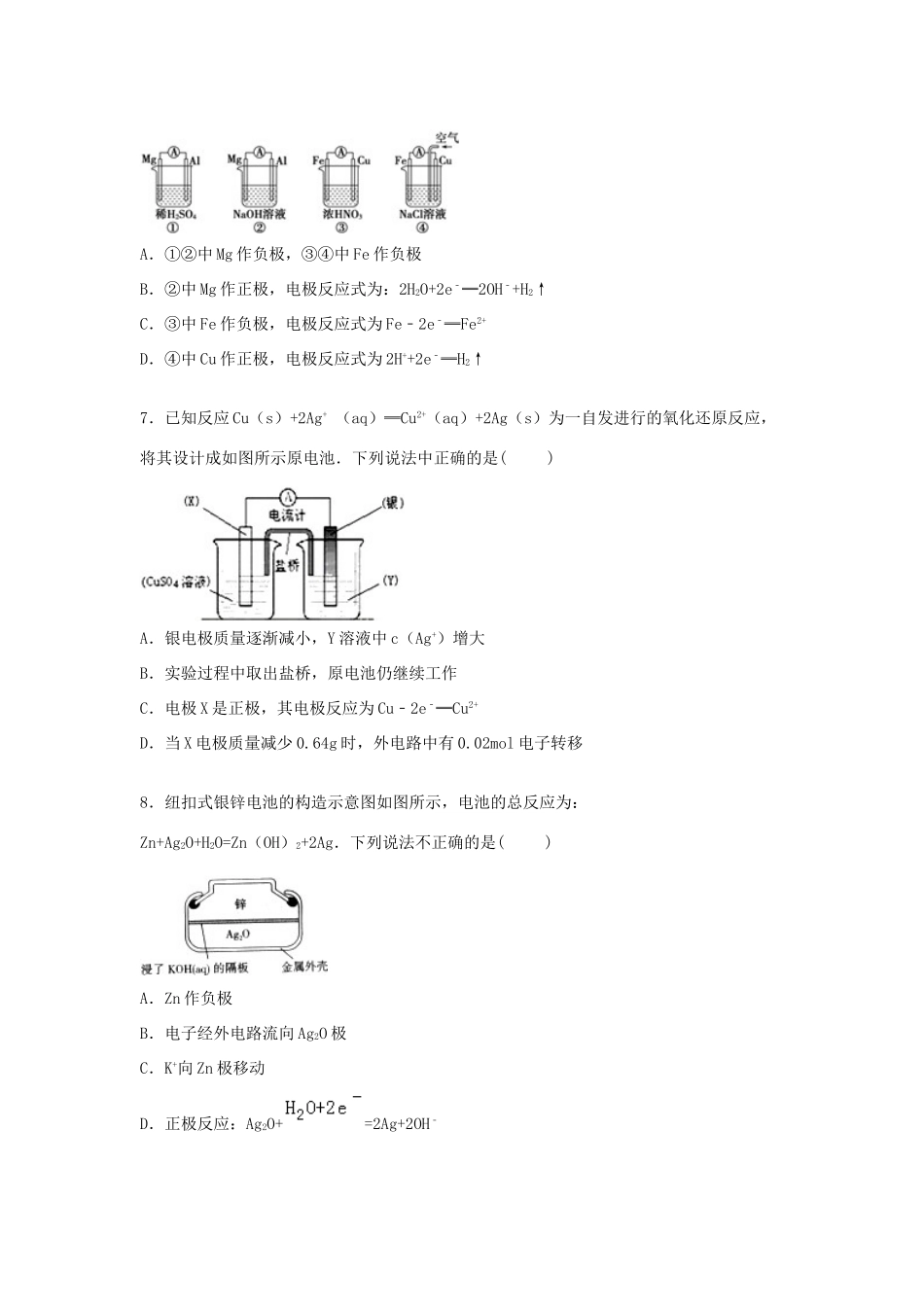
2014-2015学年重庆市七校联考高一(下)期中化学试卷一、选择题,共16小题,每小题3分,共48分,每小题只有一个选项符合题意.1.据科学家预测,月球的土壤中吸附着数百万吨的23He,每百吨23He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以24He的形式存在.下列说法中正确的是()A.24He原子核内含有4个质子B.24He和23He互为同位素C.23He原子核内含有3个中子D.24He的最外层电子数为2,故24He具有较强的金属性2.某主族元素R的原子其电子式可用表示.该元素组成的以下物质,其分子式肯定错误的是()A.最高价氧化物分子式为R2O5B.含氧酸分子式为HRO3C.含氧酸分子式为H3RO4D.气态氢化物分子式为RH53.下列表达正确的是()A.NaCl的电子式:B.CO2的分子模型示意图:C.CrO5的结构式为:该氧化物中Cr为+6价D.次氯酸的结构式:H﹣Cl﹣O4.下列设备工作时,将化学能转化为热能的是()A.硅太阳能电池B.锂离子电池C.太阳能集热器D.燃气灶5.某反应由两步反应A⇌B⇌C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是()A.两步反应均为吸热反应B.三种化合物中C最稳定C.加入催化剂会改变反应的焓变D.整个反应中△H=E1﹣E46.原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关.下列说法中正确的是()A.①②中Mg作负极,③④中Fe作负极B.②中Mg作正极,电极反应式为:2H2O+2e﹣═2OH﹣+H2↑C.③中Fe作负极,电极反应式为Fe﹣2e﹣═Fe2+D.④中Cu作正极,电极反应式为2H++2e﹣═H2↑7.已知反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)为一自发进行的氧化还原反应,将其设计成如图所示原电池.下列说法中正确的是