1科学探究1
兴趣小组的同学在课外阅读时发现:金属钠的氧化物——过氧化钠(Na2O2)是一种化学性质活泼的淡黄色固体,在常温下能跟许多物质发生化学反应放出氧气
例如:2Na2O2+2CO22Na2CO3+O2,2Na2O2+2H2O4NaOH+O2↑等,于是同学们将一小块过氧化钠投入一定质量的MgCl2溶液中,充分反应后过滤,得到无色滤液和白色固体,并对滤液的成分进行了探究
【提出问题】滤液中溶质的成分是什么
【猜想与假设】猜想一:NaCl猜想二:猜想三:NaCl、MgCl2猜想四:NaCl、MgCl2、NaOH小芳同学提出猜想四不合理,理由是
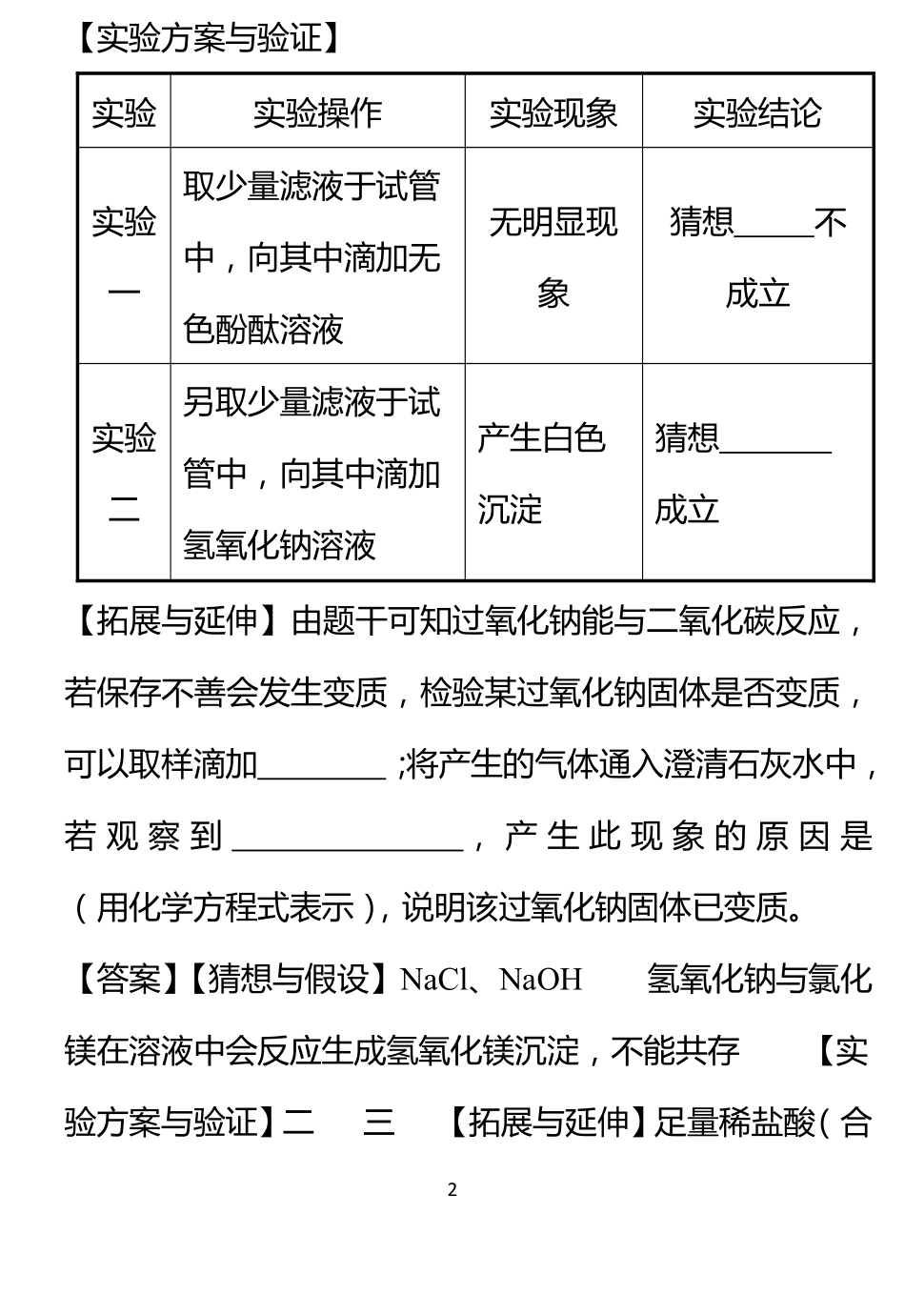
2【实验方案与验证】实验实验操作实验现象实验结论实验一取少量滤液于试管中,向其中滴加无色酚酞溶液无明显现象猜想不成立实验二另取少量滤液于试管中,向其中滴加氢氧化钠溶液产生白色沉淀猜想成立【拓展与延伸】由题干可知过氧化钠能与二氧化碳反应,若保存不善会发生变质,检验某过氧化钠固体是否变质,可以取样滴加;将产生的气体通入澄清石灰水中,若观察到,产生此现象的原因是(用化学方程式表示),说明该过氧化钠固体已变质
【答案】【猜想与假设】NaCl、NaOH氢氧化钠与氯化镁在溶液中会反应生成氢氧化镁沉淀,不能共存【实验方案与验证】二三【拓展与延伸】足量稀盐酸(合3理即可)澄清石灰水变浑CO2+Ca(OH)2CaCO3↓+H2O2
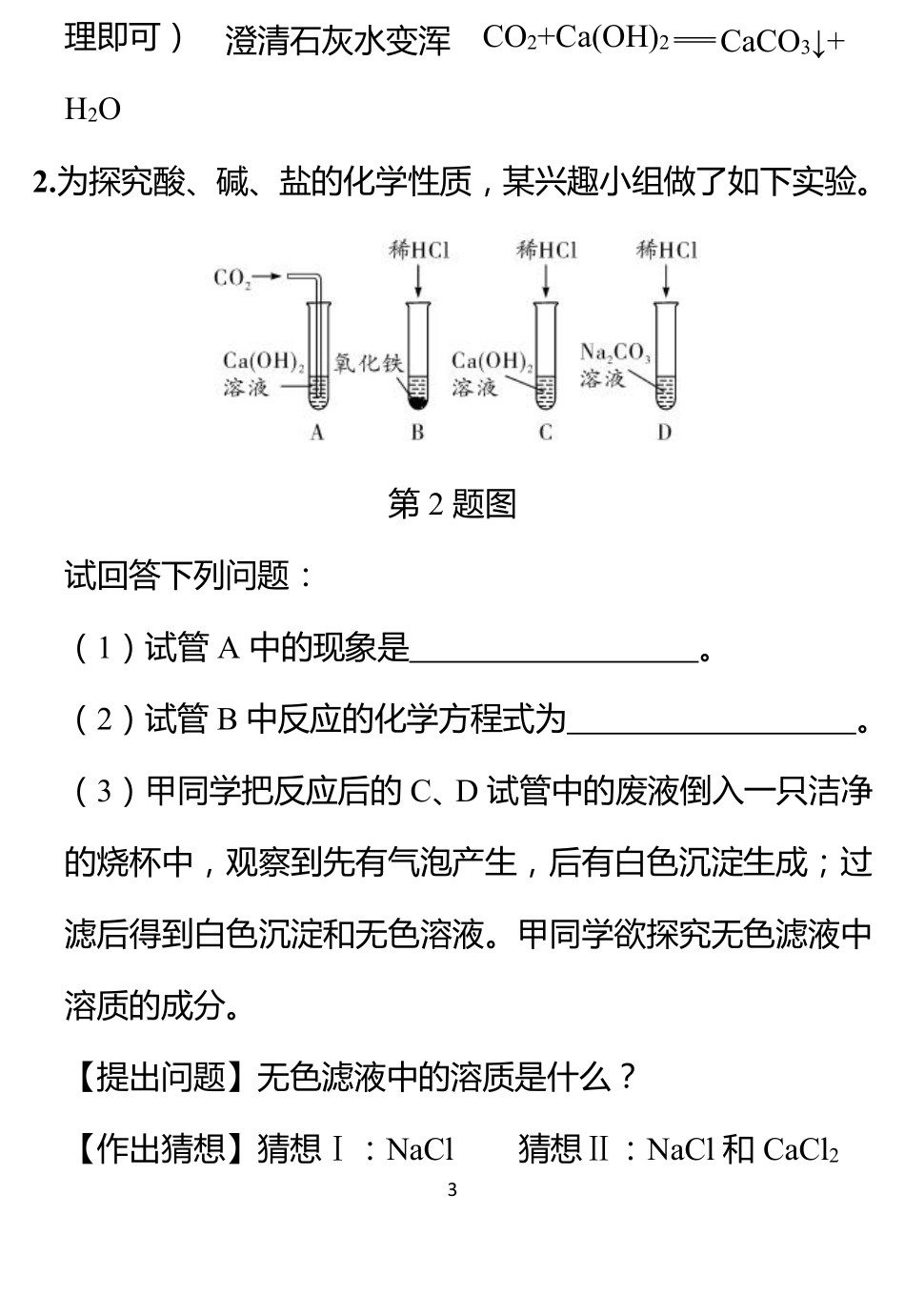
为探究酸、碱、盐的化学性质,某兴趣小组做了如下实验
第2题图试回答下列问题:(1)试管A中的现象是
(2)试管B中反应的化学方程式为
(3)甲同学把反应后的C、D试管中的废液倒入一只洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成;过滤后得到白色沉淀和无色溶液
甲同学欲探究无色滤液中溶质的成分
【提出问题】无色滤液中的溶质是什么
【作出猜想】猜想Ⅰ:NaCl猜想Ⅱ:NaCl和CaCl24猜想Ⅲ:NaCl和Na2CO3猜想