江苏省 2013-2014 学年高中化学 专题二 3
1 化学能转化为电能同步导学案 苏教版必修 2一:学习目标1
理解原电池的工作原理,掌握构成原电池的条件;2
能写出电极反应和电池反应方程式
并能判断电子流向,电解质中的离子移动方向
了解常见化学电源
能写出常见化学电源的电极反应式
二:课前预习1
原电池的概念:把______ __能转化为______ __能的装置2
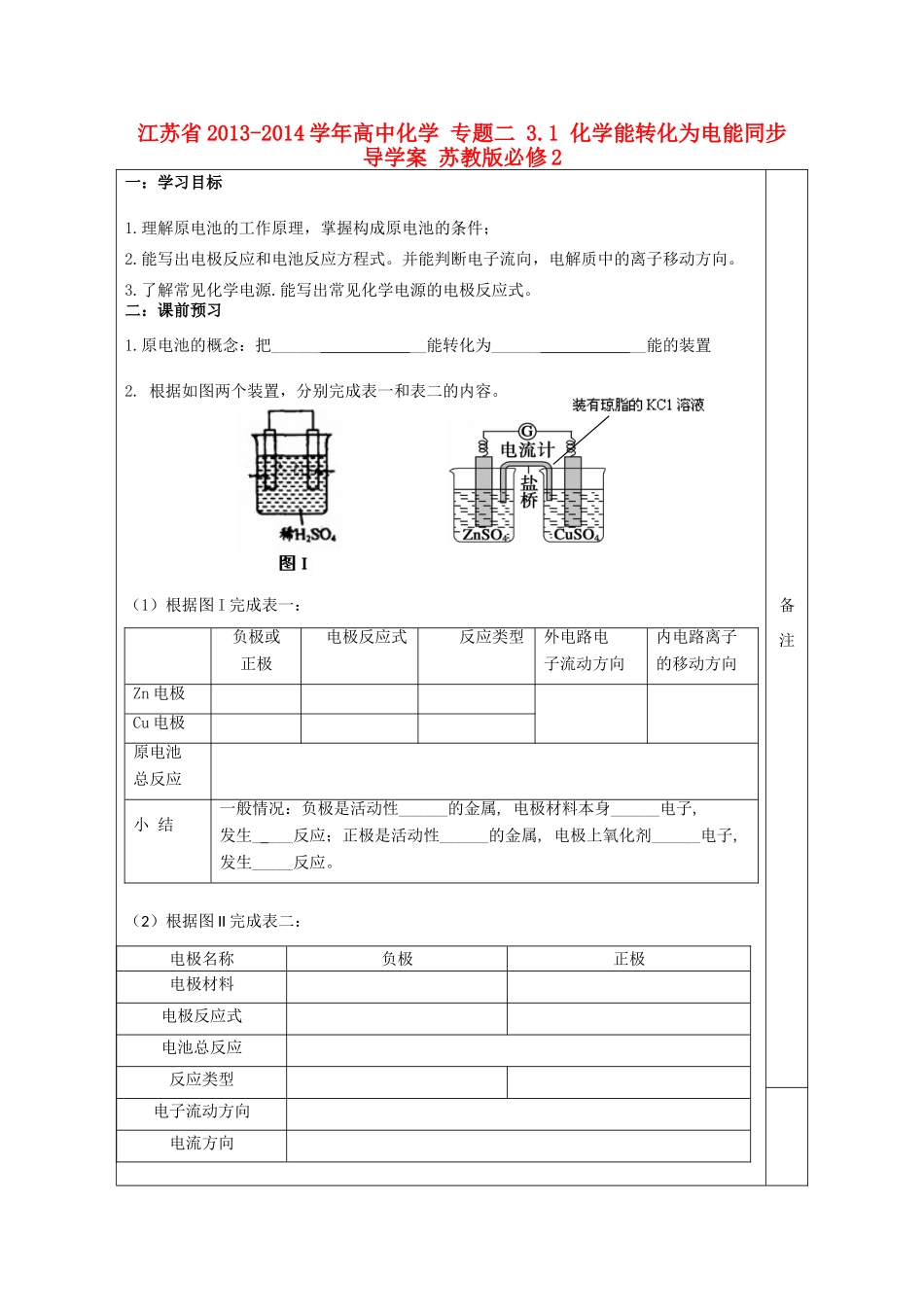
根据如图两个装置,分别完成表一和表二的内容
(1)根据图 I 完成表一:(2)根据图 II 完成表二:电极名称负极正极电极材料电极反应式电池总反应反应类型电子流动方向电流方向备注负极或正极电极反应式 反应类型外电路电子流动方向内电路离子的移动方向Zn 电极Cu 电极原电池总反应小 结一般情况:负极是活动性______的金属, 电极材料本身______电子,发生_ ___反应;正极是活动性______的金属, 电极上氧化剂______电子,发生_____反应
盐桥中离子的移向盐桥中的 Cl-移向 极,K+移向 极
三、课堂研讨1
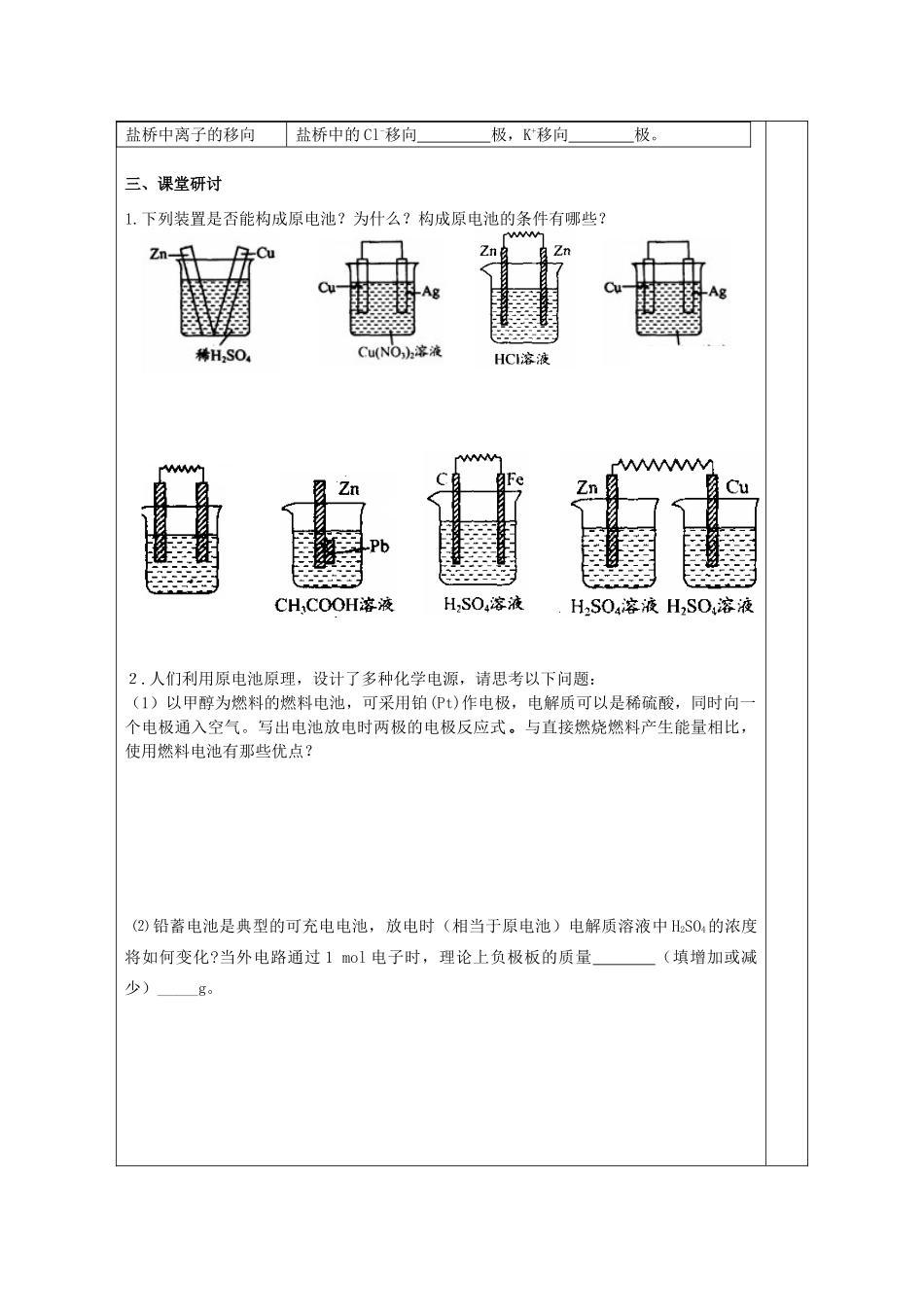
下列装置是否能构成原电池
构成原电池的条件有哪些
人们利用原电池原理,设计了多种化学电源,请思考以下问题:(1)以甲醇为燃料的燃料电池,可采用铂(Pt)作电极,电解质可以是稀硫酸,同时向一个电极通入空气
写出电池放电时两极的电极反应式
与直接燃烧燃料产生能量相比,使用燃料电池有那些优点
⑵ 铅蓄电池是典型的可充电电池,放电时(相当于原电池)电解质溶液中 H2SO4的浓度将如何变化
当外电路通过 1 mol 电子时,理论上负极板的质量 (填增加或减少)_____g
四:学后反思课堂练习—— 化学能与电能的转化 姓名: 1.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连