河南省确山县第二高级中学高中化学必修二:第一章第一节元素周期表(第二课时)【学习目标】1
了解原子结构与元素性质的关系
初步学会总结元素递变规律的能力
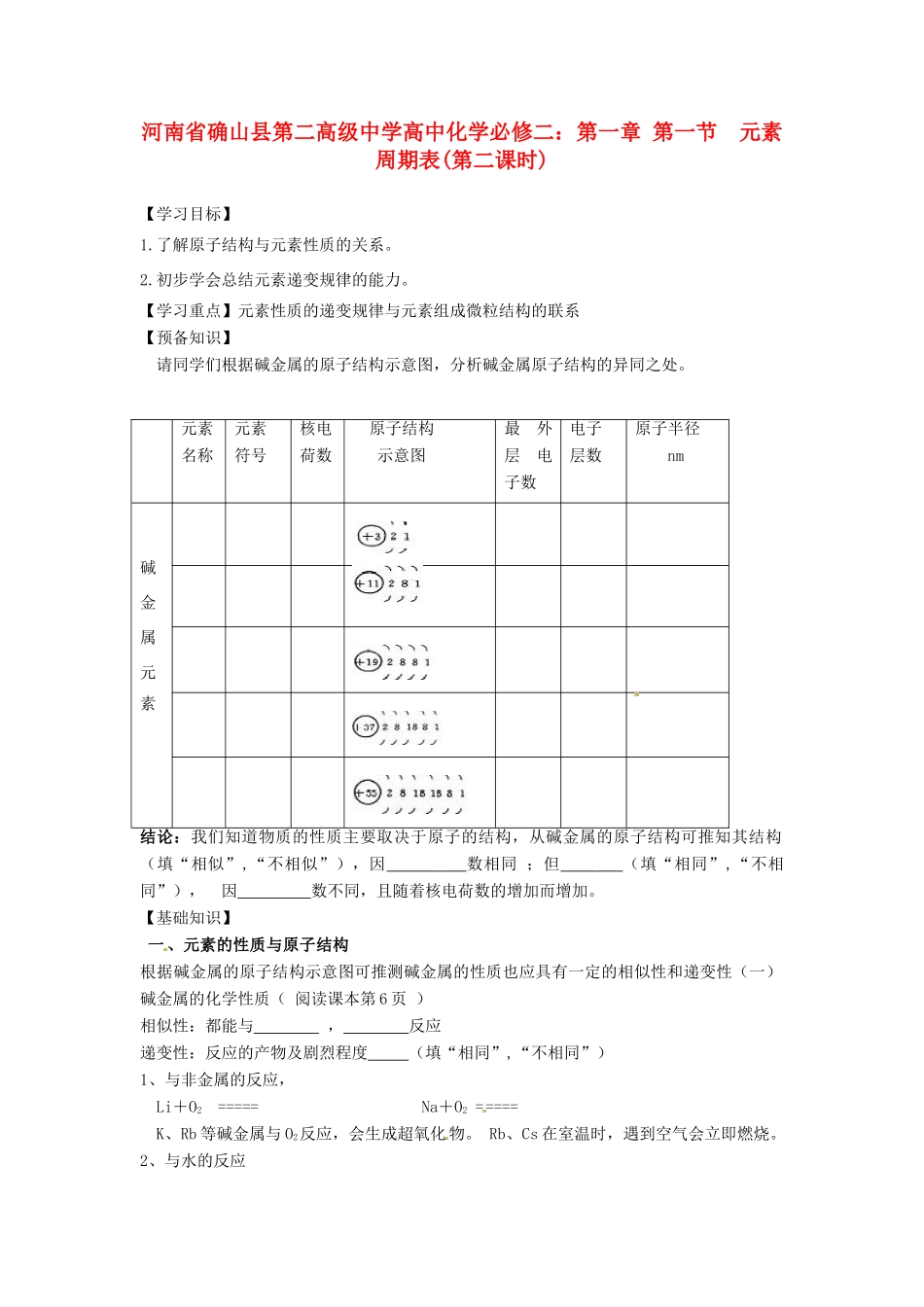
【学习重点】元素性质的递变规律与元素组成微粒结构的联系【预备知识】请同学们根据碱金属的原子结构示意图,分析碱金属原子结构的异同之处
元素名称元素符号核电荷数原子结构示意图最外层电子数电子层数原子半径nm碱金属元素结论:我们知道物质的性质主要取决于原子的结构,从碱金属的原子结构可推知其结构(填“相似”,“不相似”),因数相同;但(填“相同”,“不相同”),因数不同,且随着核电荷数的增加而增加
【基础知识】一、元素的性质与原子结构根据碱金属的原子结构示意图可推测碱金属的性质也应具有一定的相似性和递变性(一)碱金属的化学性质(阅读课本第6页)相似性:都能与,反应递变性:反应的产物及剧烈程度(填“相同”,“不相同”)1、与非金属的反应,Li+O2=====Na+O2=====K、Rb等碱金属与O2反应,会生成超氧化物
Rb、Cs在室温时,遇到空气会立即燃烧
2、与水的反应Na+H2O=====K+H2O=====除Na、K外,其他碱金属元素也都可以和水反应生成相应的碱与H2,且碱性越来越强,反应也越来越剧烈[课堂练习1]:钫(Fr)具有放射性,它是碱金属元素中最重的元素,下列预言错误的是:A
在碱金属中它具有最大的原子半径B
它的氢氧化物化学式为FrOH是一种极强的碱C
钫在空气中燃烧时,只生成化学式为Fr2O的氧化物D
它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸(二)碱金属的物理性质的比较(见课本第7页)相似性:颜色呈色(除铯略带金色光泽),都较柔软有延展性,密度,熔点,导电性和导热性也都很好
递变性:随着核电荷数的增加,密度逐渐,熔、沸点逐渐(三)卤素单质的物理性质(见课本第8页)[思考与交流]请大家根据卤素单质