高中化学必修1双向细目表章节容(知识点)知道了解理解应用第一章认识化学科学1
研究物质性质的方法和程序√2、钠、氯气的物理性质√3、钠及其氧化物、氯气的化学性质
物质的量、摩尔质量的概念既简单计算√5.物质的量浓度及其简单计算,溶液稀释时有关的计算√6.气体摩尔体积及其简单计算√7.配制一定物质的量浓度的溶液√8.物质的质量、摩尔质量、物质的量、物质的粒子数、物质的量浓度之间的相互关系及有关计算√第二章元素与物质的分类1、物质分类√2、分散系√3、丁达尔效应√4、胶体的渗析、胶体的吸附作用√5
电离方程式的书写√6、离子共存、离子的物质的量浓度√7、Cl-、SO42-、CO32-的检验方法√8.氧化还原反应、氧化、还原、氧化剂、还原剂等概念√9.简单的氧化还原反应方程式的配平、标出电子转移的方向和数目√第三章自然界中的元素1、同素异形体的概念,√2、碳酸钠和碳酸氢钠的主要性质
√3、碳单质、一氧化碳、二氧化碳、碳酸盐、碳酸氢盐之间的转化
√4.自然界中的氮循环及人类活动对氮循环的影响;√5、生物固氮和人工固氮形式,认识N2、NO、NO2的性质;√6、NH3性质及制取、铵盐的性质及铵态氮肥的使用问题;√7、HNO3的性质
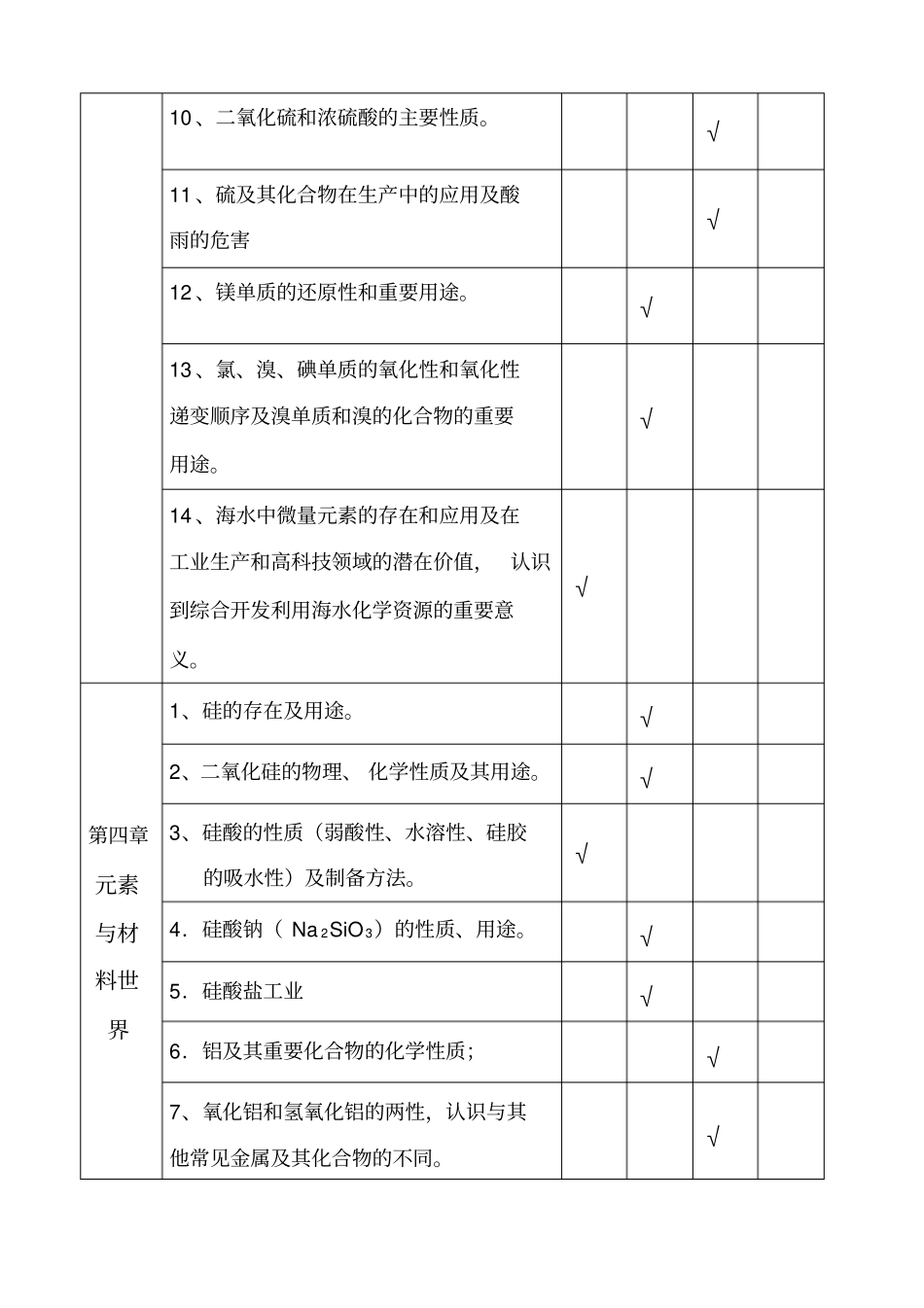
√8、硫的主要性质;√9、不同价态硫元素之间的相互转化√10、二氧化硫和浓硫酸的主要性质
√11、硫及其化合物在生产中的应用及酸雨的危害√12、镁单质的还原性和重要用途
√13、氯、溴、碘单质的氧化性和氧化性递变顺序及溴单质和溴的化合物的重要用途
√14、海水中微量元素的存在和应用及在工业生产和高科技领域的潜在价值,认识到综合开发利用海水化学资源的重要意义
√第四章元素与材料世界1、硅的存在及用途
√2、二氧化硅的物理、化学性质及其用途
√3、硅酸的性质(弱酸性、水溶性、硅胶的吸水性)及制备方法
√4.硅酸钠(Na2SiO3)的性质、用途
√5.硅酸盐