气体的制备[考纲要求]:掌握常见气体的实验室制法(包括所用试剂、仪器、反应原理和收集方法)
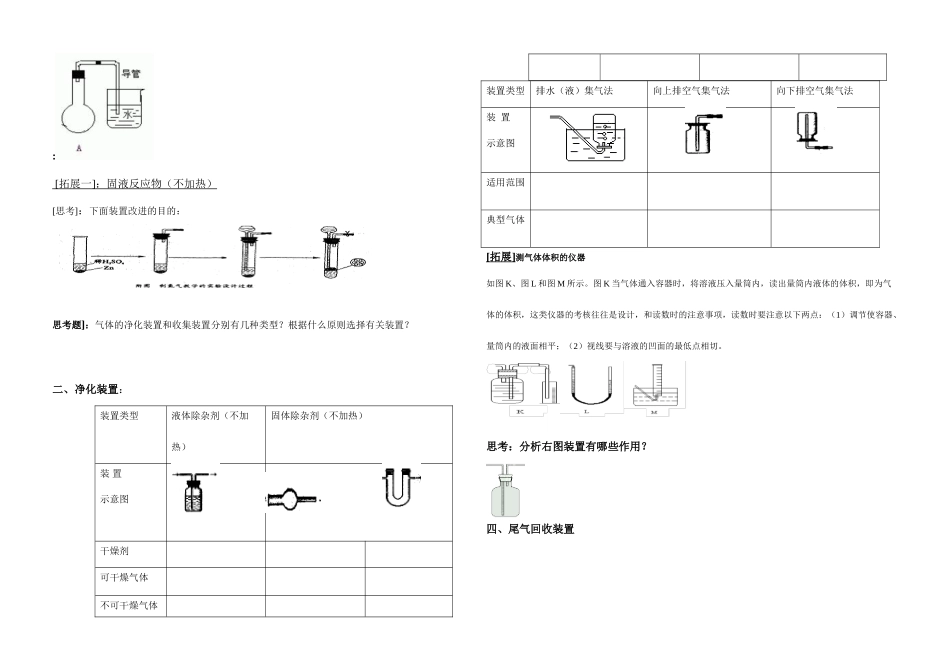
[提问]:如右图1.这套装置在实验室用于制取什么气体
2.要制得纯净的氯气,请说明B、C、D、E各装置应盛装的试剂及其作用是什么
[交流与思考]实验室用甲酸与浓硫酸在加热条件下制取CO气体,反应为:HCOOHH2O+CO↑,请设计一装置以制取干燥纯净的CO气体(画出简易图)
[提问]通过上述2例可以看出,实验室制取纯净的气体一般有几个环节
归纳总结:常见气体物质制备的基本实验流程[思考题]:如何选择气体的发生装置
气体制备的发生装置有几种类型
气体发生装置的设计原则2
气体发生装置的基本类型一、气体发生装置:装置类型固体反应物(加热)固液反应物(不加热)固液(液液)反应物(加热)装置示意图典型气体注意事项思考:装置气密性检查操作所依据的原理:规律总结:装置气密性检查操作方法:[拓展一]:固液反应物(不加热)[思考]:下面装置改进的目的:思考题]:气体的净化装置和收集装置分别有几种类型
根据什么原则选择有关装置
二、净化装置:装置类型液体除杂剂(不加热)固体除杂剂(不加热)装置示意图干燥剂可干燥气体不可干燥气体装置类型排水(液)集气法向上排空气集气法向下排空气集气法装置示意图适用范围典型气体[拓展]测气体体积的仪器如图K、图L和图M所示
图K当气体通入容器时,将溶液压入量筒内,读出量筒内液体的体积,即为气体的体积,这类仪器的考核往往是设计,和读数时的注意事项,读数时要注意以下两点:(1)调节使容器、量筒内的液面相平;(2)视线要与溶液的凹面的最低点相切
思考:分析右图装置有哪些作用
四、尾气回收装置[拓展]防止倒吸装置的改进制取气体装置收集方法反应方程式检验方法干燥尾气处理Cl2HClNaCl+H2SO4(浓)═HCl↑+NaHSO4湿润的蓝色石蕊试纸变红O2NH3H2CO2[小结