学必求其心得,业必贵于专精专题10
7化学实验方案的设计与评价1.下列实验方案可行的是()A.用1mol/L的盐酸与MnO2反应制取氯气B.用湿润的淀粉碘化钾试纸鉴别二氧化氮和溴蒸气C.用10mL量筒量取8
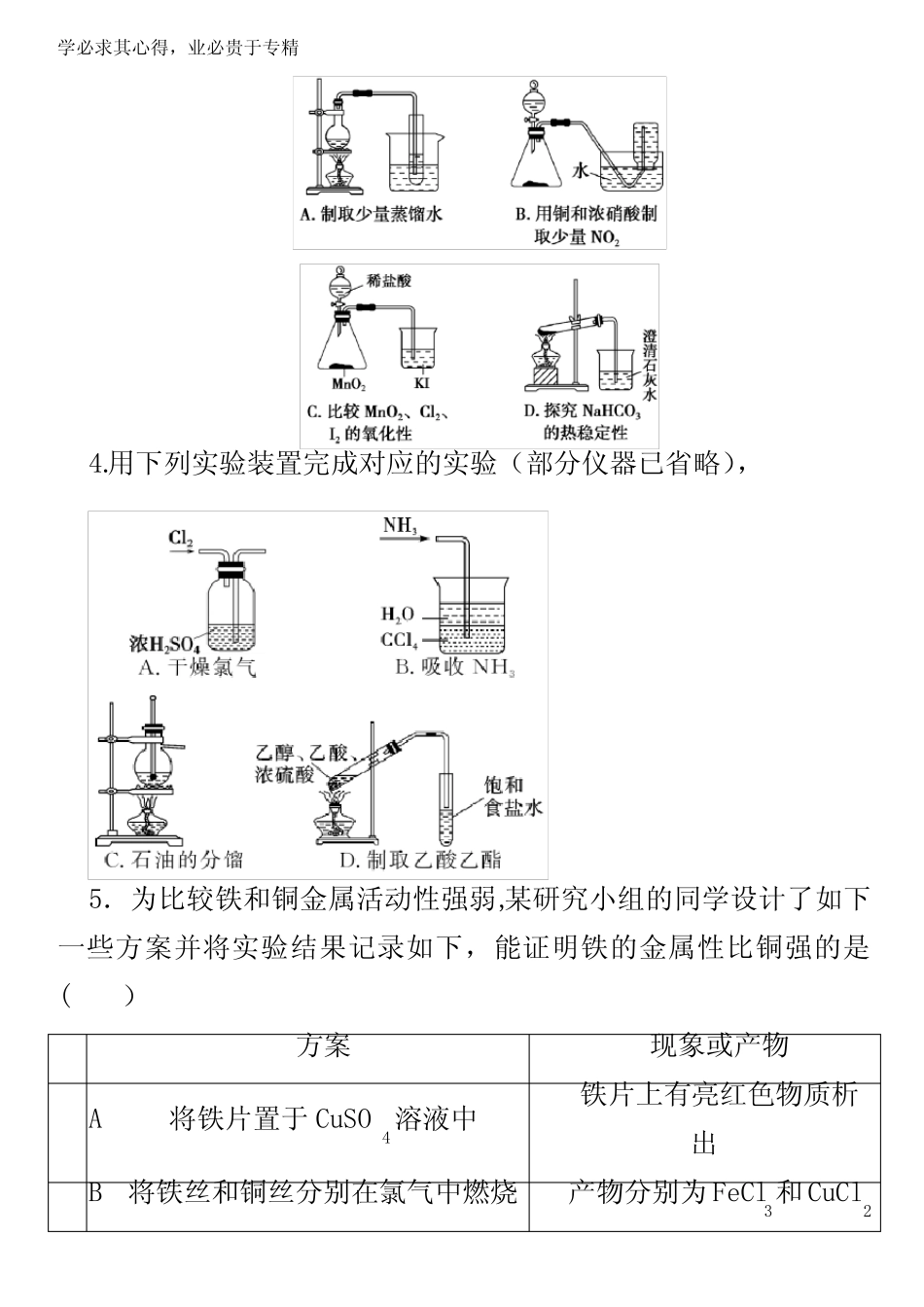
50mL浓硫酸用于配制一定物质的量浓度的稀硫酸D.用湿润的有色纸条鉴别氯化氢和氯气2.某同学设计了如图实验装置探究硝酸的性质,根据图示判断下列结论不正确的是()A.试管内壁上的“黄霜”的成分是硫B.该实验既说明了浓硝酸具有氧化性,又说明了浓硝酸具有挥发性C.烧杯内氢氧化钠溶液的作用是除去尾气,防止尾气污染环境D.试管中浓硝酸可以用浓盐酸代替3.下列实验方案正确且能达到相应实验目的的是()学必求其心得,业必贵于专精4
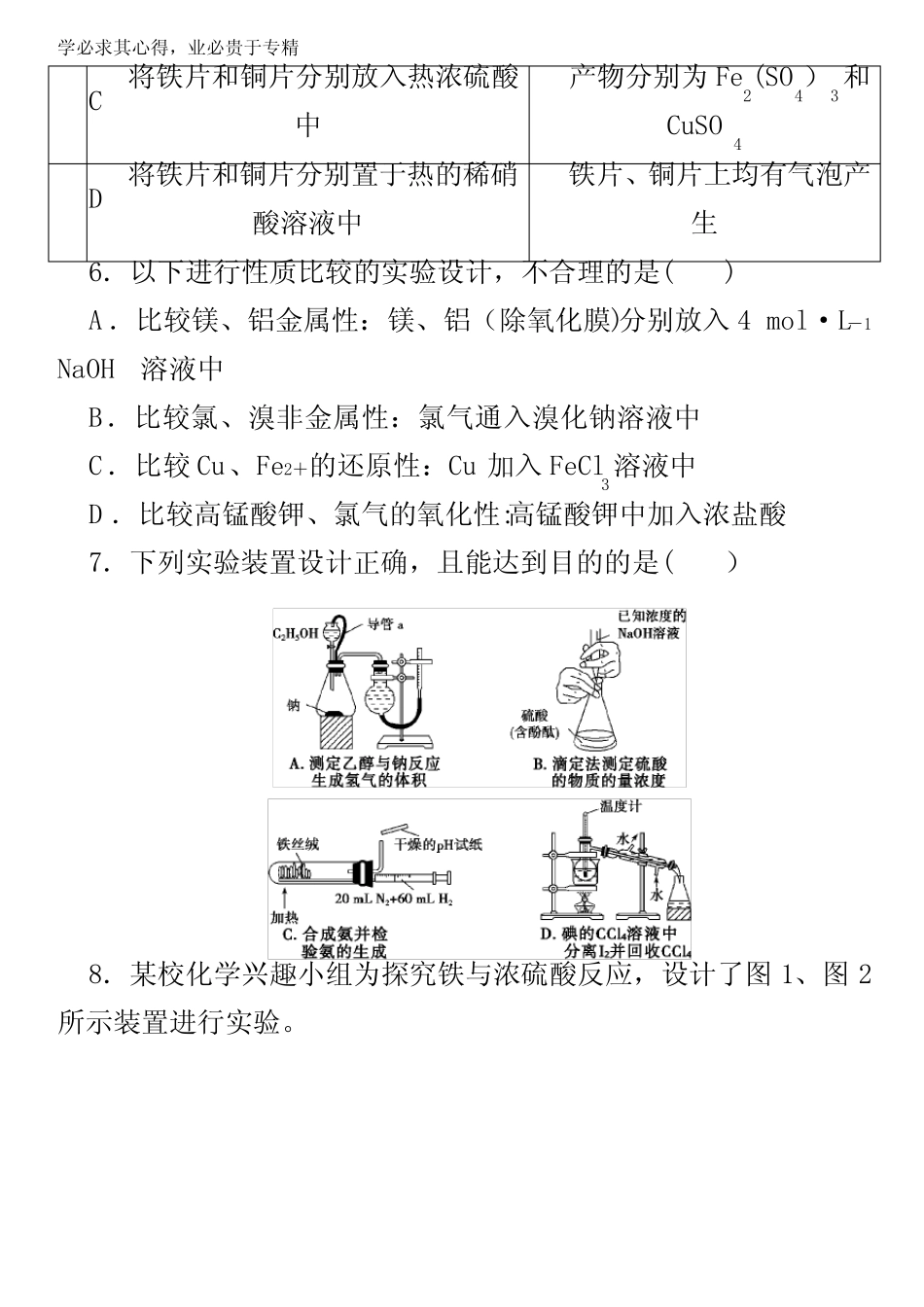
用下列实验装置完成对应的实验(部分仪器已省略),5.为比较铁和铜金属活动性强弱,某研究小组的同学设计了如下一些方案并将实验结果记录如下,能证明铁的金属性比铜强的是()方案现象或产物A将铁片置于CuSO4溶液中铁片上有亮红色物质析出B将铁丝和铜丝分别在氯气中燃烧产物分别为FeCl3和CuCl2学必求其心得,业必贵于专精C将铁片和铜片分别放入热浓硫酸中产物分别为Fe2(SO4)3和CuSO4D将铁片和铜片分别置于热的稀硝酸溶液中铁片、铜片上均有气泡产生6.以下进行性质比较的实验设计,不合理的是()A.比较镁、铝金属性:镁、铝(除氧化膜)分别放入4mol·L-1NaOH溶液中B.比较氯、溴非金属性:氯气通入溴化钠溶液中C.比较Cu、Fe2+的还原性:Cu加入FeCl3溶液中D.比较高锰酸钾、氯气的氧化性:高锰酸钾中加入浓盐酸7.下列实验装置设计正确,且能达到目的的是()8.某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验
学必求其心得,业必贵于专精(1)比较两实验装置,图2所示装置的优点是:①能更好地吸收有毒气体SO2,防止其污染环境;②__