课时1原子核外电子的排布元素周期律目标与素养:1
了解核外电子的分层排布规律及表示方法
(微观探析与模型认知)2
了解元素的原子结构与性质的周期性变化规律,理解元素周期律的内容及实质
(宏观辨识与证据推理)一、原子核外电子排布1.电子层的划分(1)核外电子的能量及运动区域(2)电子层及其与能量的关系各电子层(由内到外)序号(n)1234567符号KLMNOPQ与原子核的距离由近到远能量由低到高2.核外电子的排布规律(1)电子总是尽可能地先从内层排起,当一层充满后再填充下一层,即原子核外电子排布时,先排K层,充满后再填充L层
(2)原子核外各电子层最多容纳2n2个电子
(3)原子最外层电子数不能超过8(K层为最外层时不能超过2),次外层电子数不能超过18
违背了哪些规律
[答案]能量最低原理,最外层电子不超过8个
二、元素周期律1.原子核外电子排布的周期性变化(1)第一周期最外层电子数由1→2
(2)第二周期最外层电子数由1→8
(3)第三周期最外层电子数由1→8
规律:随着原子序数的递增,元素原子的最外层电子数呈现1~8的周期性变化(第一周期除外)
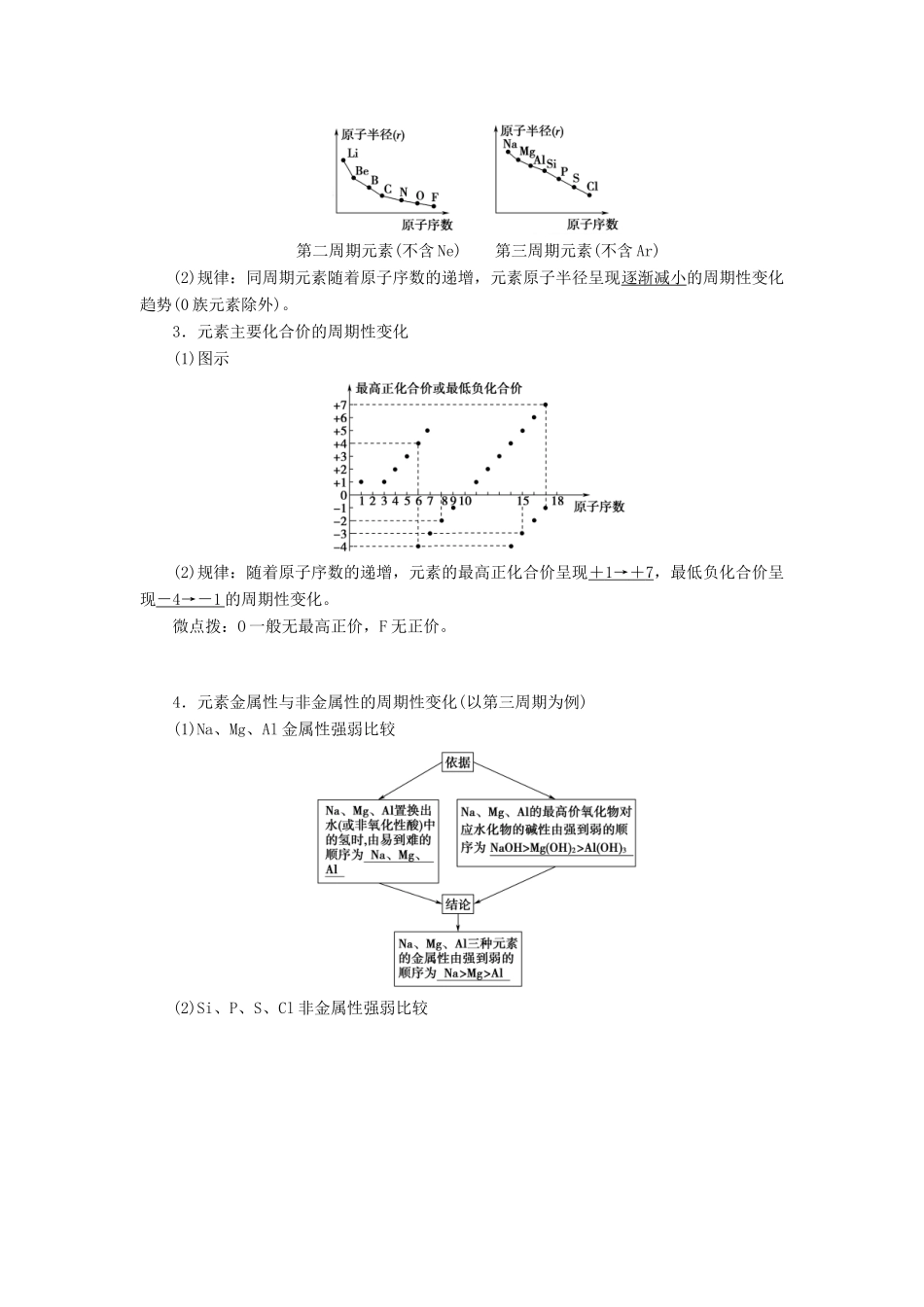
2.元素原子半径的周期性变化(1)图示第二周期元素(不含Ne)第三周期元素(不含Ar)(2)规律:同周期元素随着原子序数的递增,元素原子半径呈现逐渐减小的周期性变化趋势(0族元素除外)
3.元素主要化合价的周期性变化(1)图示(2)规律:随着原子序数的递增,元素的最高正化合价呈现+1→+7,最低负化合价呈现-4→-1的周期性变化
微点拨:O一般无最高正价,F无正价
4.元素金属性与非金属性的周期性变化(以第三周期为例)(1)Na、Mg、Al金属性强弱比较(2)Si、P、S、Cl非金属性强弱比较(3)同周期元素性质的递变规律随着原子序数的递增5.元素周期律(1)内容:元素的性质随着原子序数的递增而呈周期性变化
(2)实质:元素性质