滚动加练2化学基本理论综合应用1.(·苏北三市一调)氢气是清洁的能源,也是重要的化工原料
(1)以H2为原料制取氨气进而合成CO(NH2)2的反应如下:N2(g)+3H2(g)===2NH3(g)ΔH=-92
4kJ·mol-12NH3(g)+CO2(g)===NH2CO2NH4(s)ΔH=-159
47kJ·mol-1NH2CO2NH4(s)===CO(NH2)2(s)+H2O(I)ΔH=+72
49kJ·mol-1则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为____________________________________________________________
(2)已知叠氮酸(HN3)不稳定,同时也能与活泼金属反应,反应方程式为:2HN3===3N2↑+H2↑2HN3+Zn===Zn(N3)2+H2↑2molHN3与过量Zn完全反应,在标准状况下生成67
2L气体,其中N2的物质的量为__________________
(3)用丙烷和水为原料在电催化下制氢气,同时得到一种含有三元环的环氧化合物A,则该反应的化学方程式为_______________________________
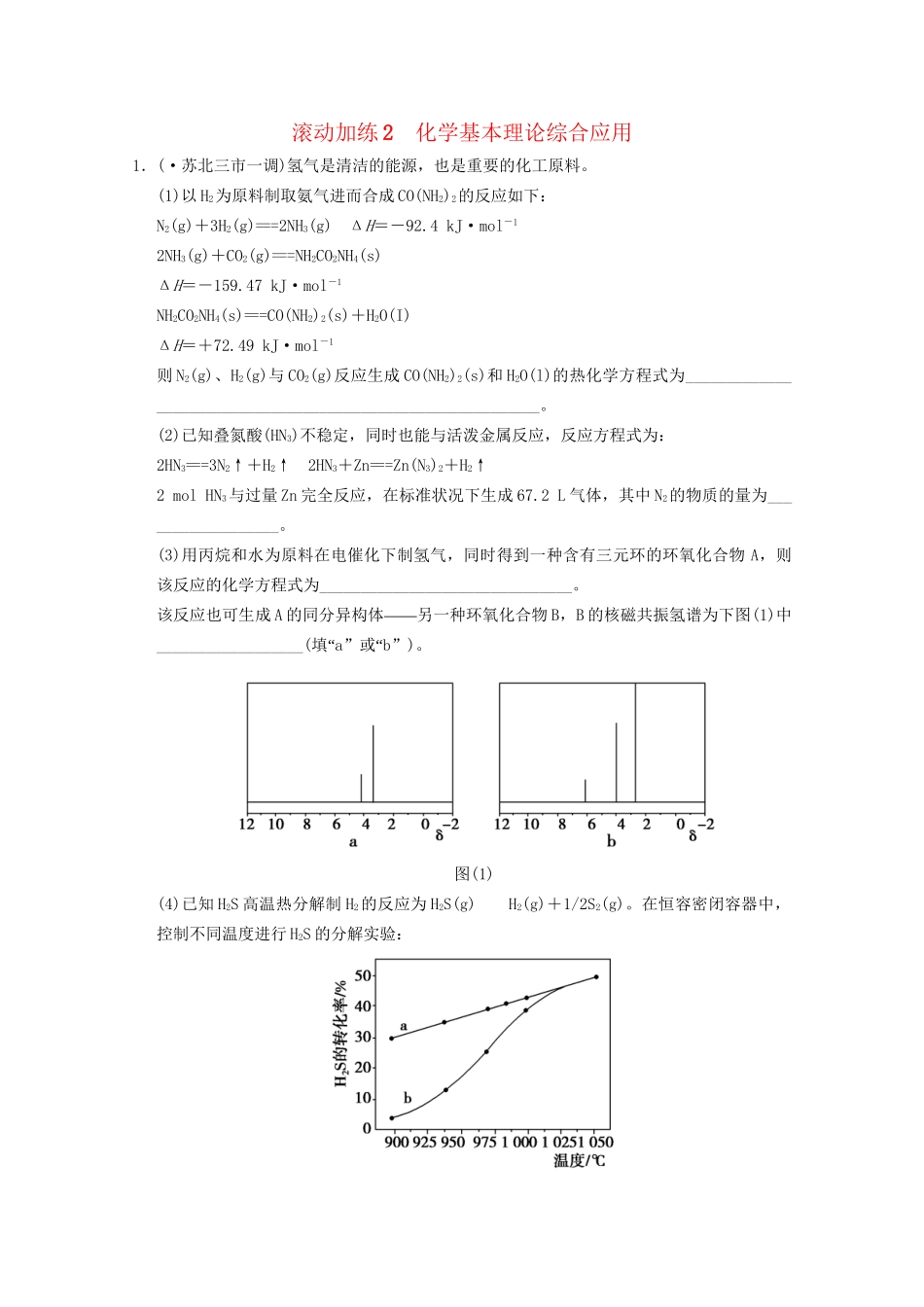
该反应也可生成A——的同分异构体另一种环氧化合物B,B的核磁共振氢谱为下图(1)中__________________(“填a”“或b”)
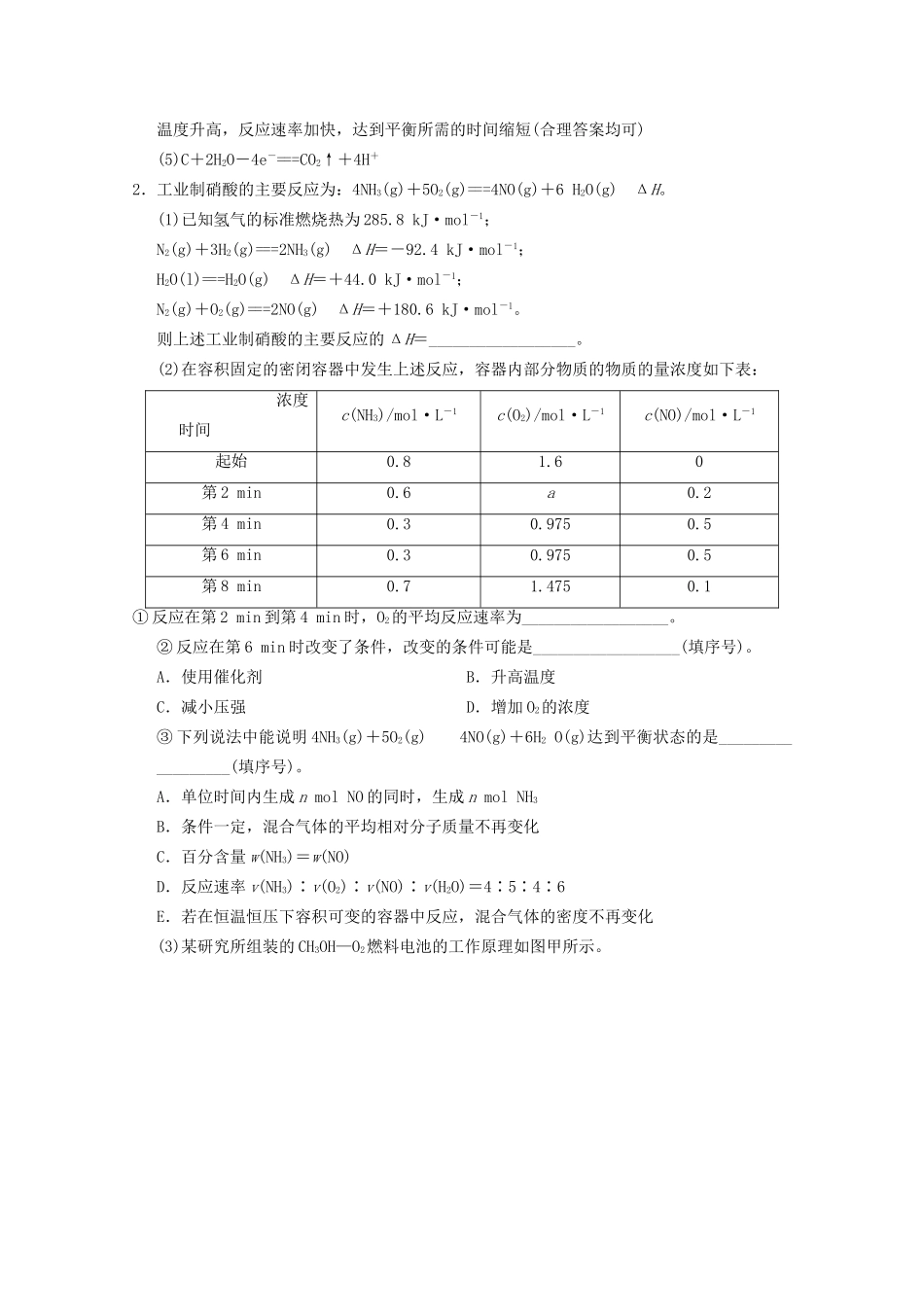
图(1)(4)已知H2S高温热分解制H2的反应为H2S(g)H2(g)+1/2S2(g)
在恒容密闭容器中,控制不同温度进行H2S的分解实验:图(2)以H2S的起始浓度均为cmol·L-1测定H2S的转化率,结果如上图(2)所示
图中a曲线为H2S的平衡转化率与温度的关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率
若985℃时,反应经tmin达到平