课时3化学实验方案的设计与评价(时间:45分钟分值:100分)一、选择题(本题共7个小题,每题6分,共42分,每个小题只有一个选项符合题意
)1.下列相关家庭实验设计能达到预期目的的是()
相关实验预期目的A在少量食用碱中滴加食醋探究食用碱是碳酸钠还是碳酸氢钠B在食用盐中滴加少量淀粉液探究食用盐是否为加碘盐C用激光笔照射淀粉液探究淀粉液是胶体还是溶液D将鸡蛋白溶于水后,滴加AgNO3溶液验证蛋白质中含有氯元素解析碳酸钠、碳酸氢钠均能与乙酸反应生成二氧化碳,A不能达到预期目的;食用盐中加入的是化合态的碘,不能用淀粉检验,B不能达到预期目的;蛋白质不是电解质,不能电离出氯离子,D不能达到预期目的
答案C2.某同学通过实验探究硫及其化合物的性质,实验现象正确且能达到目的的是()
A.点燃硫黄,产生有刺激性气味气体,该气体可以漂白纸浆B.将CuSO4·5H2O加入浓硫酸中,蓝色晶体变为白色,说明浓硫酸具有强的脱水性C.把SO2通入盛有滴加了酚酞试剂的NaOH溶液中,溶液褪色,说明SO2具有漂白作用D.将Cu片加入浓硫酸中,反应剧烈,说明浓硫酸具有强的氧化性解析点燃硫黄生成SO2,A正确;选项B说明浓硫酸有吸水性;选项C体现了SO2的酸性氧化物的性质;Cu和浓H2SO4的反应需要加热,且根据反应的剧烈程度不能判断物质的氧化性或还原性的强弱,D错
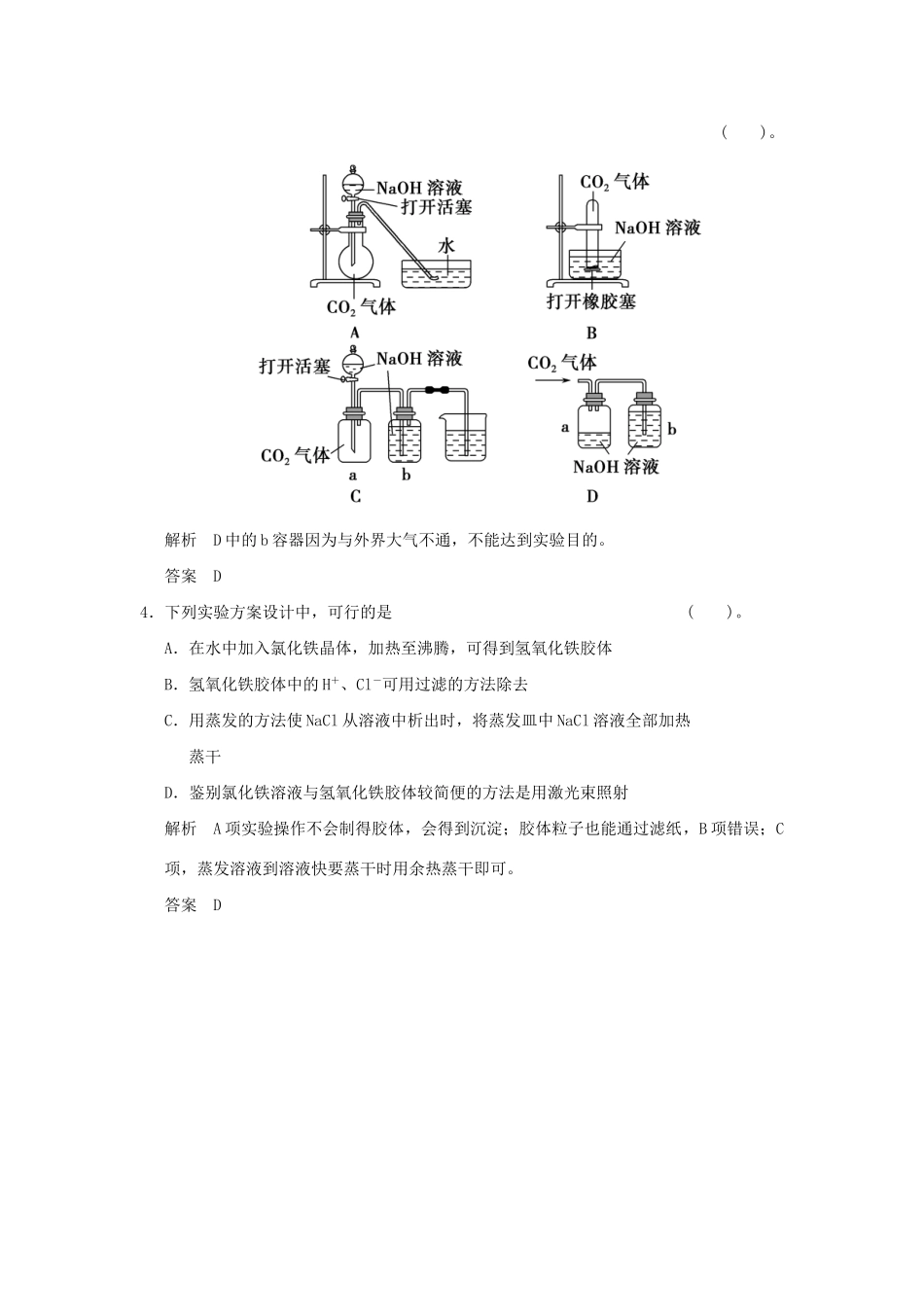
答案A3.(·潍坊模拟)某化学兴趣小组设计了下列四个实验装置,试图通过观察实验现象说明CO2与NaOH溶液发生了反应
其中无法达到实验目的的是()
解析D中的b容器因为与外界大气不通,不能达到实验目的
答案D4.下列实验方案设计中,可行的是()
A.在水中加入氯化铁晶体,加热至沸腾,可得到氢氧化铁胶体B.氢氧化铁胶体中的H+、Cl-可用过滤的方法除去C.用蒸发的方法使NaCl从溶液中析出时,将蒸发皿中NaCl溶液全部加热蒸干D.鉴别氯化铁溶液