第二节元素周期表元素周期律明考纲要求理主干脉络1
掌握元素周期律的实质
了解元素周期表(长式)的结构(周期、族)及其应用
了解金属、非金属在元素周期表中的位置及其性质的递变规律
以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系
以ⅠA族和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系
一、元素周期表1
原子序数按照元素在周期表中的顺序给元素所编的序号
原子序数=核电荷数=质子数=核外电子数
编排原则横行→周期纵行→族3
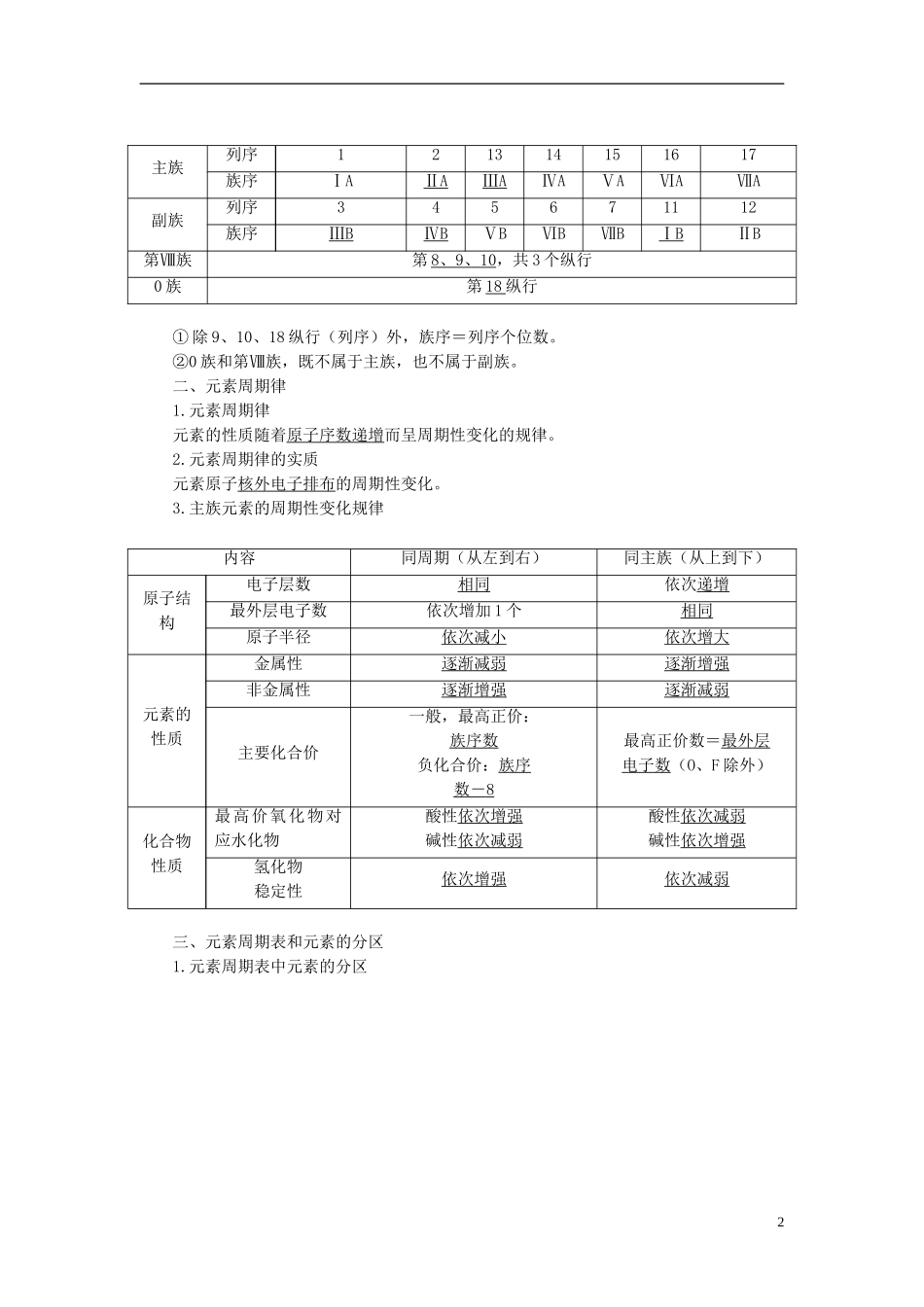
结构(1)周期(7个横行,7个周期):(2)族(18个纵行,16个族)1主族列序121314151617族序ⅠAⅡAⅢAⅣAⅤAⅥAⅦA副族列序345671112族序ⅢBⅣBⅤBⅥBⅦBⅠBⅡB第Ⅷ族第8、9、10,共3个纵行0族第18纵行①除9、10、18纵行(列序)外,族序=列序个位数
②0族和第Ⅷ族,既不属于主族,也不属于副族
二、元素周期律1
元素周期律元素的性质随着原子序数递增而呈周期性变化的规律
元素周期律的实质元素原子核外电子排布的周期性变化
主族元素的周期性变化规律内容同周期(从左到右)同主族(从上到下)原子结构电子层数相同依次递增最外层电子数依次增加1个相同原子半径依次减小依次增大元素的性质金属性逐渐减弱逐渐增强非金属性逐渐增强逐渐减弱主要化合价一般,最高正价:族序数负化合价:族序数-8最高正价数=最外层电子数(O、F除外)化合物性质最高价氧化物对应水化物酸性依次增强碱性依次减弱酸性依次减弱碱性依次增强氢化物稳定性依次增强依次减弱三、元素周期表和元素的分区1
元素周期表中元素的分区2分界线两侧的元素,既能表现出一定的非金属性,又能表现出一定的金属性
元素周期表和元素周期律应用的重要意义(1)科学预测:为新元素的发现及预测它们的原子结构和性质提供线索
(2)寻找新材料:将下面左右两侧