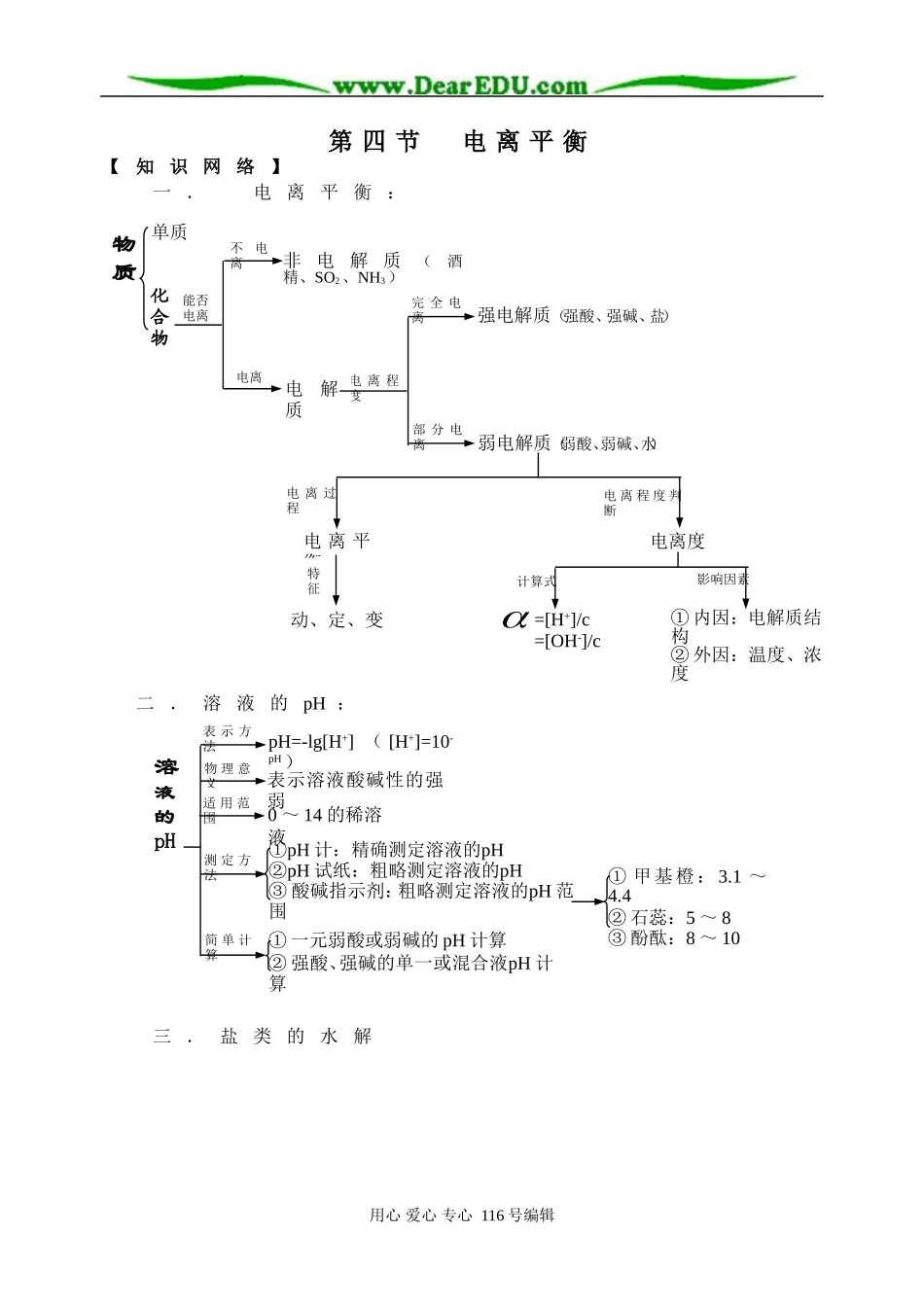
第四节电离平衡【知识网络】一.电离平衡:二.溶液的pH:三.盐类的水解用心爱心专心116号编辑强电解质(强酸、强碱、盐)化合物能否电离物质单质电离程度电离不电离非电解质(酒精、SO2、NH3)电解质完全电离部分电离弱电解质(弱酸、弱碱、水)①内因:电解质结构②外因:温度、浓度电离平衡电离过程电离程度判断电离度动、定、变特征计算式=[H+]/c=[OH-]/c影响因素①一元弱酸或弱碱的pH计算②强酸、强碱的单一或混合液pH计算①甲基橙:3
4②石蕊:5~8③酚酞:8~10①pH计:精确测定溶液的pH②pH试纸:粗略测定溶液的pH③酸碱指示剂:粗略测定溶液的pH范围0~14的稀溶液表示溶液酸碱性的强弱溶液的pH表示方法物理意义适用范围测定方法简单计算pH=-lg[H+]([H+]=10-pH)四.中和滴定用心爱心专心116号编辑①判断离子浓度;②判断离子共存;③判断弱电解质强弱;④盐溶液配制;⑤物质的鉴别与除杂;⑥制备胶体;⑦明矾净水;⑧泡沫灭火机原理、草木灰不能与铵态氮肥混合使用;⑨试剂存放:如NH4F溶液不能用玻璃瓶保存;⑩判断水解盐受热产物内因:水解生成的弱电解质“越弱”,水解程度越大外因:①温度:升温有利水解;②浓度:越稀越水解;③外加酸或碱:抑制或促进水解①为可逆反应;②水解程度是微弱的单离子水解:①水写分子式(不能写成H+或OH-),中间用可逆(用不能用=),后无沉气出(不能用↑、↓);②多元弱酸根要分步写;③阳离子水解一般一步写离子方程式书写是水的电离平衡发生移动,改变了[H+]与[OH-]相对大小,使溶液呈酸性或碱性实质类型规律特征影响因素应用盐类水解①强酸强碱盐—只溶解,不水解,溶液呈中性②强碱弱酸盐—多元弱酸根分步水解,溶液呈碱性③强酸弱碱盐—阳离子水解,溶液呈酸性④弱酸弱碱盐—水解后溶液的酸碱性由弱酸根和弱碱的相对强弱决定⑤完全水解—有沉淀、气体