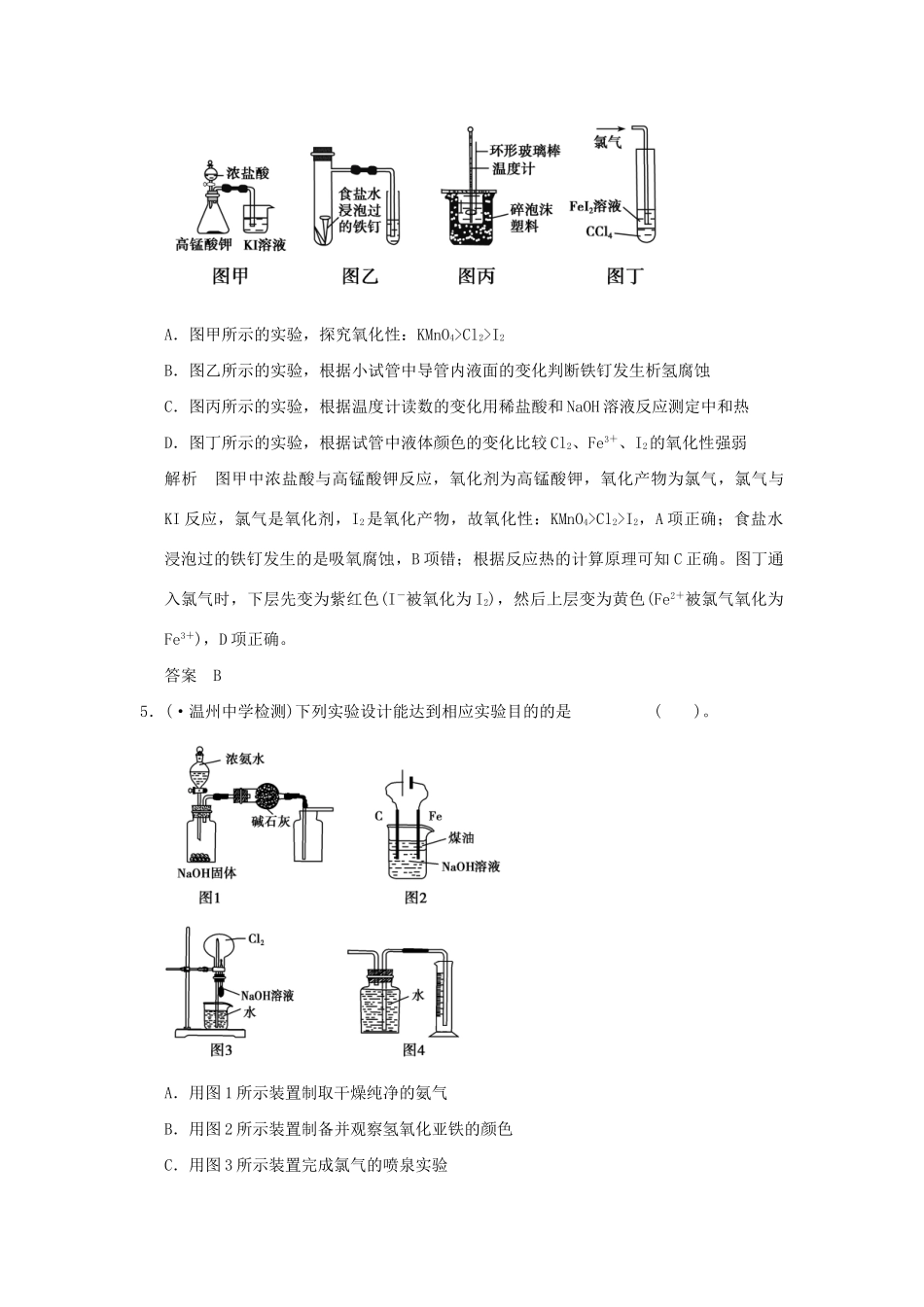
滚动加练4化学实验综合提升练1.(·四川理综,4)下列实验方案中,不能达到实验目的的是()
选项实验目的实验方案A检验CH3CH2Br在NaOH溶液中是否发生水解将CH3CH2Br与NaOH溶液共热
冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀B检验Fe(NO3)2晶体是否已氧化变质将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红C验证Br2的氧化性强于I2将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色D验证Fe(OH)3的溶解度小于Mg(OH)2将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色解析A项,用稀HNO3酸化后,加入AgNO3溶液,有淡黄色AgBr沉淀生成,即说明原反应液中有Br-产生,由此可以证明CH3CH2Br在NaOH溶液中发生了水解,正确;B项,NO在酸性条件下具有强氧化性,能够氧化Fe2+生成Fe3+,故滴加KSCN溶液后溶液变红色,不能证明Fe(NO3)2是否氧化变质,错误;C项,CCl4溶液显紫色,说明有I2生成,即发生反应:2KI+Br2===2KBr+I2,从而证明Br2的氧化性强于I2,正确;D项,沉淀由白色变为红褐色,说明Mg(OH)2转化成了Fe(OH)3,根据沉淀的转化规律,故可以说明Fe(OH)3的溶解度小于Mg(OH)2,正确
答案B2.(·衢州中学检测)大多数药品在实验室中必须密封保存,防止被空气中的氧气氧化而变质
下列括号内的物质是用来检验括号外的药品是否变质的试剂,其中变质原因属于氧化还原反应,而且括号内的试剂能够检验括号外的药品是否变质的是()
A.Na2SO3(BaCl2)B.FeCl2(KSCN)C.KI(氯水)D.NaOH(盐酸)解析该题考查了物质的检验,从深层意义上考查了药品保存的原理