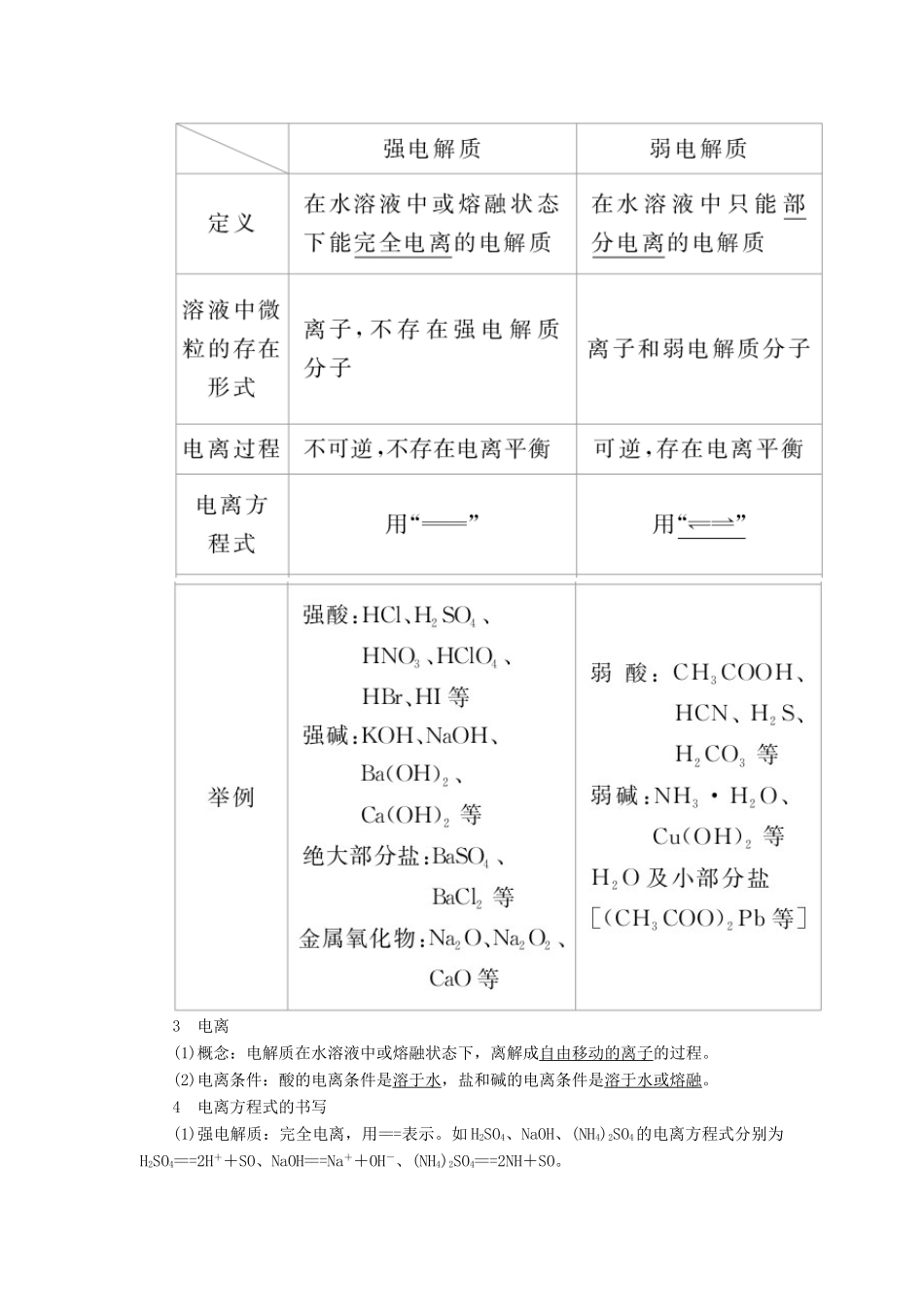
1 电解质和非电解质2 强电解质和弱电解质3 电离(1)概念:电解质在水溶液中或熔融状态下,离解成自由移动的离子的过程
(2)电离条件:酸的电离条件是溶于水,盐和碱的电离条件是溶于水或熔融
4 电离方程式的书写(1)强电解质:完全电离,用===表示
如 H2SO4、NaOH、(NH4)2SO4的电离方程式分别为H2SO4===2H++SO、NaOH===Na++OH-、(NH4)2SO4===2NH+SO
(2)弱电解质:部分电离,用表示
① 多元弱酸分步电离,且电离程度逐步减弱,酸性主要由第一步电离决定
如 H2S 的电离方程式为 H2SH++HS-,HS-H++S2-
② 多元弱碱分步电离,但一步写出
如 Cu(OH)2Cu2++2OH-
③ 两性氢氧化物双向电离
如 Al(OH)3的电离方程式:H++AlO+H2OAl(OH)3Al3++3OH-
(3)酸式盐① 强 酸 酸 式 盐 完 全 电 离 , 一 步 到 底
如 NaHSO4 在 水 溶 液 中 的 电 离 方 程 式 为 NaHSO4===Na++H++SO,在熔融状态下的电离方程式为 NaHSO4===Na++HSO
② 多元弱酸酸式盐,第一步完全电离,其余部分电离
如 NaHCO3===Na++HCO,HCOH++CO
5 离子共存(1)本质所谓几种离子在同一溶液中能大量共存,就是指离子之间不发生任何反应;若离子之间能发生反应,则不能大量共存
(2)常见的限制条件学霸巧学卡 正确理解电解质等概念(1)电解质和非电解质均是化合物,单质和混合物既不是电解质,也不是非电解质
(2)电解质不一定导电,如固态 NaCl、液态 HCl 等;导电物质不一定是电解质,如铁、铝等金属单质
(3)电解质一定是指自身电离生成离子的化合物,有些化合物的水溶液能导电,但溶液中的离子不是它自身电离产