专题19无机非金属材料的主角——硅【知识回放】1.碳和硅在自然界中以什么形式存在
2.CO2的物理性质:是一种色体,溶于水,固态CO2俗称
3.完成以下方程式:(1)CO2+H2O→(2)CO2+NaOH→(3)CO2+CaO→4.请写出硅原子和碳原子的原子结构示意图
5.根据Na2CO3+SiO2Na2SiO3+CO2↑能说明硅酸酸性比碳酸强吗
6.由于SiO2既可与碱反应,也可与氢氟酸反应,所以SiO2为两性氧化物,这种说法是否正确
【答案】1.碳在自然界中有游离态和化合态两种形式存在,硅在自然界中以化合态存在
2.无色无味气体能干冰3.(1)CO2+H2O=H2CO3(2)CO2+2NaOH=Na2CO3+H2O(3)CO2+CaO=CaCO34.【新知精讲】一、二氧化硅1
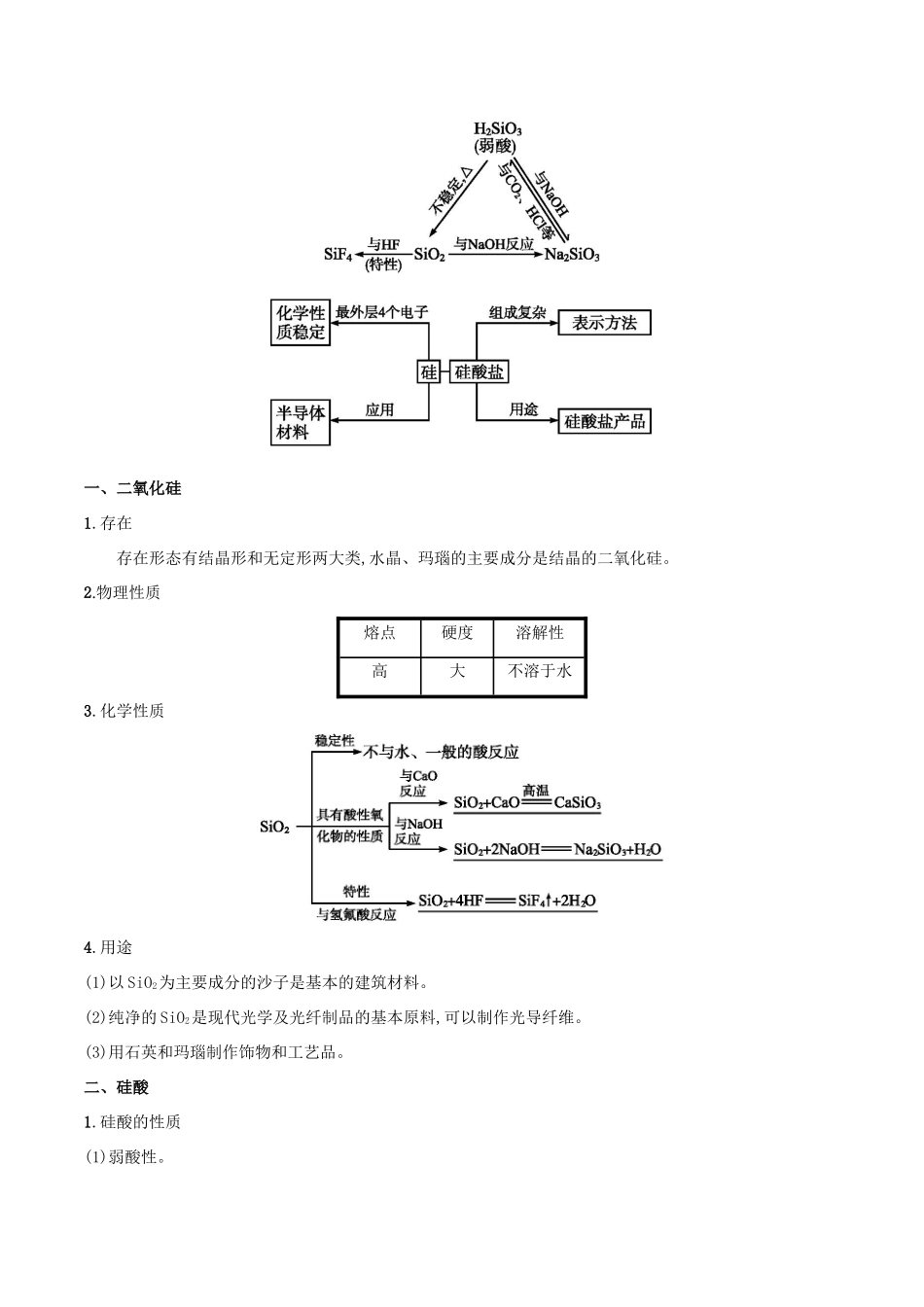
存在存在形态有结晶形和无定形两大类,水晶、玛瑙的主要成分是结晶的二氧化硅
物理性质熔点硬度溶解性高大不溶于水3
用途(1)以SiO2为主要成分的沙子是基本的建筑材料
(2)纯净的SiO2是现代光学及光纤制品的基本原料,可以制作光导纤维
(3)用石英和玛瑙制作饰物和工艺品
硅酸的性质(1)弱酸性
向Na2SiO3溶液中通入CO2,反应的化学方程式为Na2SiO3+CO2+H2O===H2SiO3(胶体)+Na2CO3或Na2SiO3+2CO2+2H2O===H2SiO3(胶体)+2NaHCO3
结论:H2SiO3酸性比H2CO3酸性弱
(2)不稳定性
H2SiO3受热易分解,化学方程式为H2SiO3SiO2+H2O
硅酸的制备(1)Na2SiO3溶液与CO2的反应:Na2SiO3+CO2+H2O===H2SiO3(胶体)+Na2CO3
(2)Na2SiO3与盐酸的反应:Na2SiO3+2HCl===H2SiO3(胶体)+2NaCl
硅酸的存在及用途(1)浓度小时: