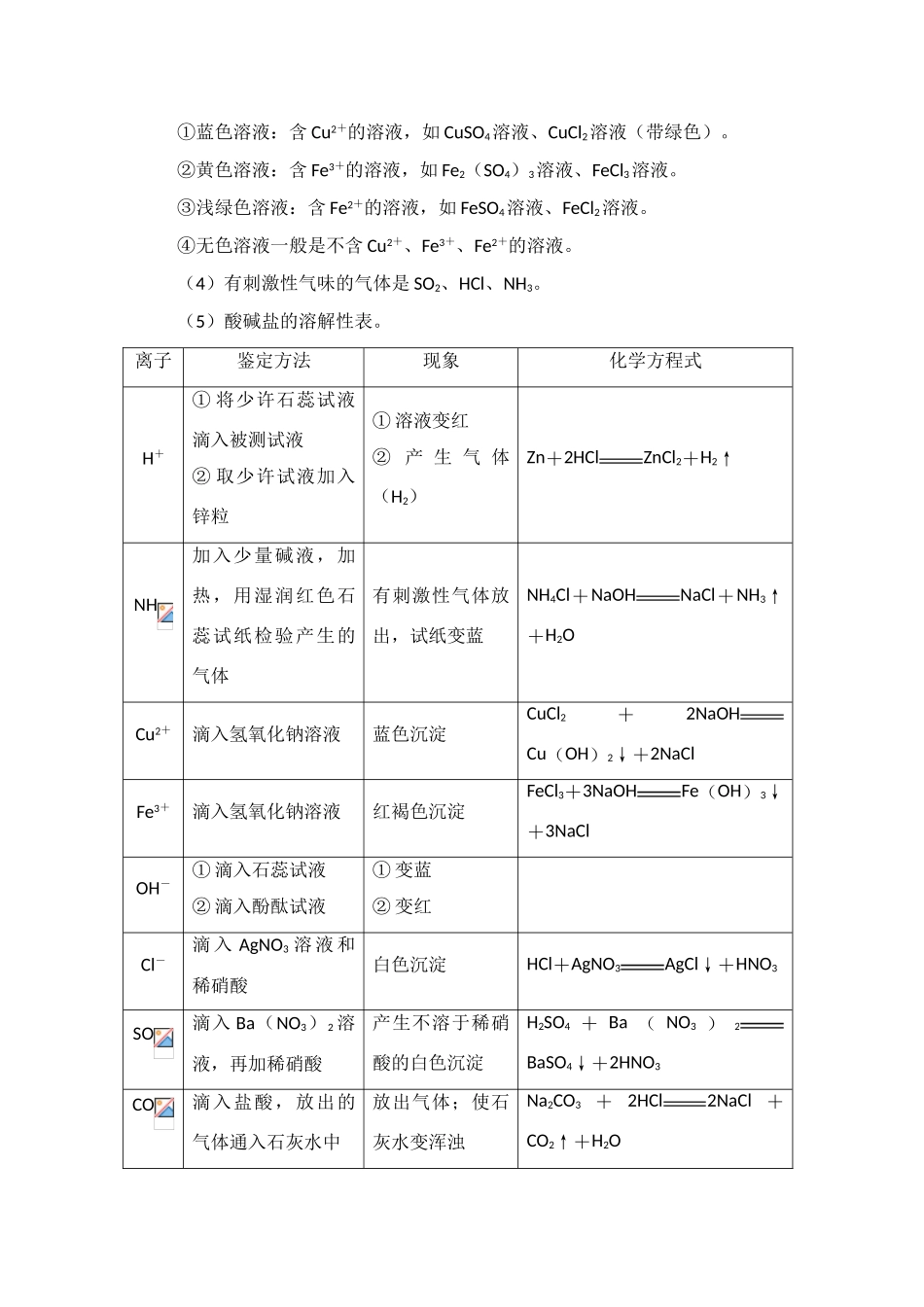
研究物质的试验方法规律总结 1.物质检验的操作步骤 (1)物理方法:依据特殊的物理性质(如颜色、气味、溶解性、溶解时的热效应等)进行观察、分析、判断,得出结论。 (2)化学方法:一般应包括取样、操作、现象、结论四个部分,要求做到: ①“先取样,后操作”,如果样品是固体,一般先用水溶解,配成溶液后再检验; ②要“各取少量溶液,分别加入几支试管”进行检验,不得在原试剂瓶中进行检验; ③要“先现象,后结论”,如向 Na2CO3溶液中滴加盐酸,所观察到的现象应记录为“有气泡产生”或“有无色气体放出”,不能说成“碳酸钠和盐酸反应,放出二氧化碳”,或“有无色二氧化碳气体放出”。 2.常见物质的主要物理特性 (1)固体物质的颜色 ①白色固体:CuSO4、MgO、P2O5、CaO、Ca(OH)2、CaCO3、KClO3、KCl、NaCl、Na2CO3 等 ②红色固体:Cu、Fe2O3 ③黑色固体:C(木炭)、CuO、MnO2、Fe3O4、铁粉④蓝色固体:CuSO4·5H2O ⑤绿色固体:Cu2(OH)2CO3 ⑥淡黄色固体:S。 (2)沉淀的颜色 ①不溶于水也不溶于稀硝酸的白色沉淀物是 AgCl、BaSO4。 ②不溶于水但能溶于酸,且能产生大量气泡,生成能使澄清石灰水变浑浊的气体的白色沉淀物常见的是 CaCO3、BaCO3、MgCO3、ZnCO3、BaSO3、CaSO3。 ③ 不 溶 于 水 , 能 溶 于 酸 , 但 没 有 气 泡 生 成 的 白 色 沉 淀 物 常 见 的 是Mg(OH)2、Zn(OH)2、Al(OH)3。 ④不溶于水的蓝色沉淀物是 Cu(OH)2。 ⑤不溶于水的红褐色沉淀是 Fe(OH)3。 (3)溶液的颜色 ①蓝色溶液:含 Cu2+的溶液,如 CuSO4溶液、CuCl2溶液(带绿色)。 ②黄色溶液:含 Fe3+的溶液,如 Fe2(SO4)3溶液、FeCl3溶液。 ③浅绿色溶液:含 Fe2+的溶液,如 FeSO4溶液、FeCl2溶液。 ④无色溶液一般是不含 Cu2+、Fe3+、Fe2+的溶液。 (4)有刺激性气味的气体是 SO2、HCl、NH3。 (5)酸碱盐的溶解性表。离子鉴定方法现象化学方程式H+① 将少许石蕊试液滴入被测试液② 取少许试液加入锌粒① 溶液变红② 产 生 气 体(H2)Zn+2HClZnCl2+H2↑NH加入少量碱液,加热,用湿润红色石蕊试纸检验产生的气体有刺激性气体放出,试纸变蓝NH4Cl+NaOHNaCl+NH3↑+H2OCu2+滴入氢氧化钠溶液蓝色沉淀CuCl2+2NaOHCu(OH)2↓+2NaClFe3+滴入氢氧化钠溶液红褐色沉淀FeCl3+3NaOHFe(OH)3↓+3NaClOH-① 滴入石蕊试液② 滴入酚酞试液① 变蓝...