第1课时原电池的工作原理发展目标体系构建1
能通过双液电池的实验探究活动,了解原电池的工作原理,能写出电极反应式和电池反应式
能利用身边的材料设计简单的原电池
提升“科学探究和创新意识”的学科素养
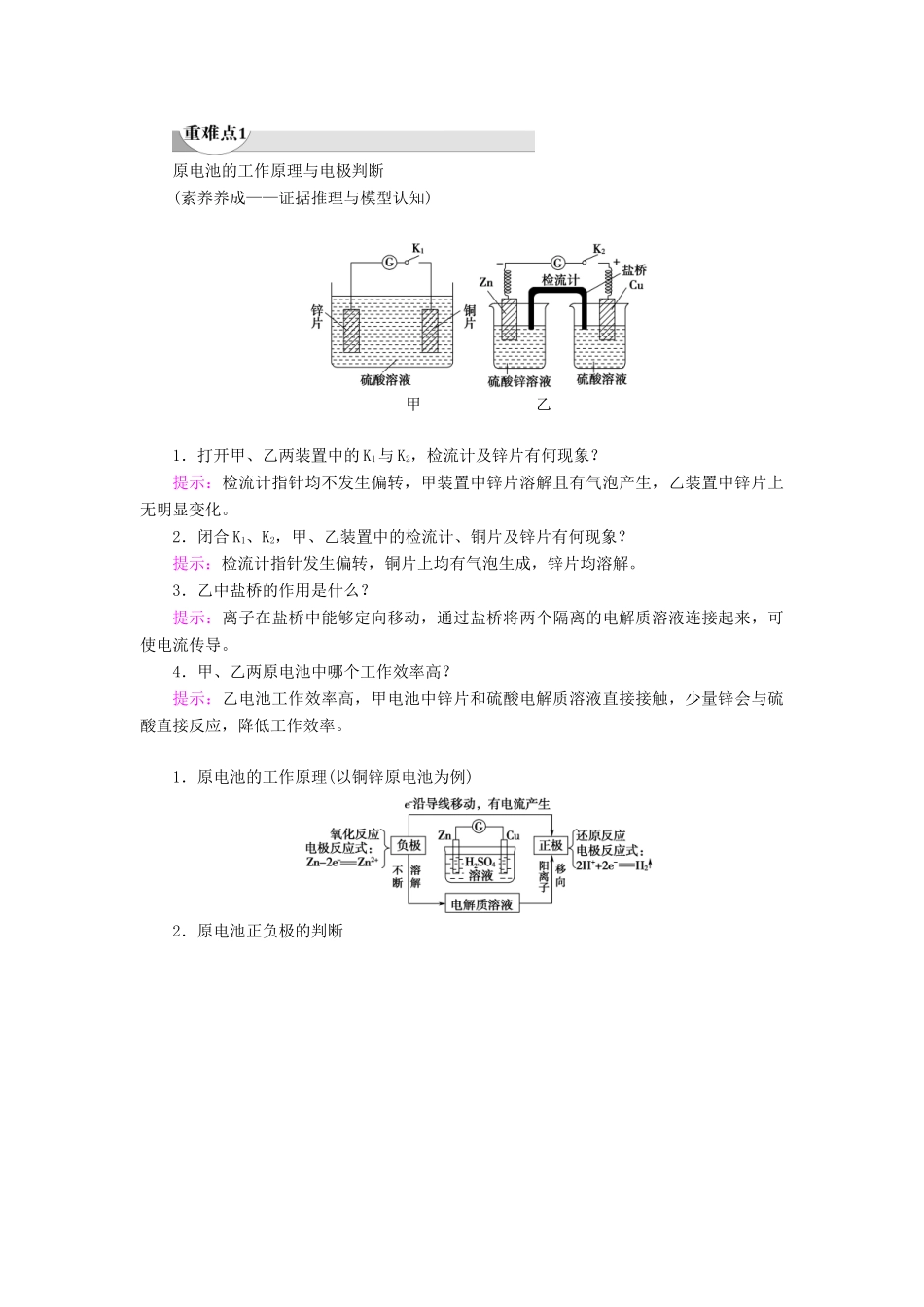
1.铜锌原电池实验探究(1)实验装置(2)实验现象检流计指针电极表面变化情况(a)发生偏转锌片质量减少,铜片质量增加(b)发生偏转锌片质量减少,铜片质量增加(3)电极材料及电极反应负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电池反应Zn+Cu2+===Cu+Zn2+电子流向由锌极通过导线流向铜极离子移向阳离子移向正极,阴离子移向负极盐桥作用构成闭合回路,使离子通过,传导电流微点拨:外电路中由电子的定向移动产生电流,而电解质溶液内部只有离子的定向移动,没有电子的移动
2.原电池的工作原理(1)原电池①定义:能把化学能转化为电能的装置
②电极名称及电极反应
负极:电子流出的一极,发生氧化反应;正极:电子流入的一极,发生还原反应
③原电池的构成条件
a.两个活泼性不同的电极(两种金属或一种金属和一种能导电的非金属)
b.将电极插入电解质溶液
c.构成闭合回路
d.能自发发生的氧化还原反应
(2)工作原理外电路中电子由负极流向正极;内电路(电解质溶液)中阴离子移向负极,阳离子移向正极;电子发生定向移动从而形成电流,实现了化学能向电能的转化
1.判断对错(对的在括号内打“√”,错的在括号内打“×”
)(1)所有的氧化还原反应都可以设计成原电池
()(2)原电池中,负极材料一定比正极材料活泼
()(3)原电池工作时,负极发生氧化反应
()(4)原电池中,电流由负极经导线流向正极
()(5)铜锌原电池中,溶液中的阳离子移向锌极
()提示:(1)×自发的氧化还原反应才能设计成原电池
(2)×原电池的负极材料不一定比正极材料活泼,